|
下列关于物质性质变化的比较,不正确的是: | |
| [ ] | |
A. |
酸性强弱:HI>HBr>HCl>HF |
B. |
原子半径大小:Na>S>O |
C. |
碱性强弱:KOH>NaOH>LiOH |
D. |
还原性强弱:F->Cl->I- |
|
在25℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,下列热化学方程式正确的是 | |
| [ ] | |
A. |
CH3OH(l)+ |
B. |
2CH3OH(l)+3O2(g) |
C. |
2CH3OH(l)+3O2(g) |
D. |
2CH3OH(l)+3O2(g) |
|
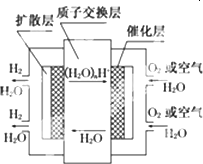
质子交换膜燃料电池的工作原理如图所示,则下列叙述不正确的是
| |
| [ ] | |
A. |
正极反应为:O2+4H++4e-=2H2O |
B. |
负极反应为:2H2-4e-=4H+ |
C. |
导电离子为质子,且在电池内部由正极定向移动至负极 |
D. |
总反应式为:2H2+O2=2H2O |
|
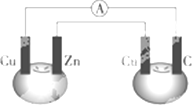
根据下列实验事实: (1)X+Y2+=X2++Y (2)Z+2H2O (3)Z2+离子的氧化性比X2+弱 (4)由Y、W作电极组成的原电池反应为:Y-2e-=Y2+ 由此可知,X、Y、Z、W的还原性由强到弱的顺序是 | |
| [ ] | |
A. |
X>Y>Z>W |
B. |
Y>X>W>Z |
C. |
Z>X>Y>W |
D. |
Z>Y>X>W |
|
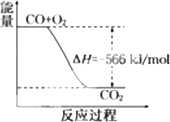
已知:2CO(g)+O2(g) Na2O2(s)+CO2(g) 根据以上热化学方程式判断,下列说法正确的是 | |
| [ ] | |
A. |
CO的燃烧热为283 kJ |
B. |
如图可表示由CO生成CO2的反应过程和能量关系
|
C. |
2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol |
D. |
CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023 |
|
同温同压下,已知下列各反应为放热反应,下列各热化学方程式中反应热最小的是 | |
| [ ] | |
A. |
2A(l)+B(l) |
B. |
2A(g)+B(g) |
C. |
2A(g)+B(g) |
D. |
2A(l)+B(l) |
|
某原电池总反应的离子方程式为:2Fe3++Fe=3Fe2+,不能实现该反应的原电池是 | |
| [ ] | |
A. |
正极为Cu,负极为Fe,电解质溶液为FeCl3 |
B. |
正极为C,负极为Fe,电解质溶液为Fe(NO3)3 |
C. |
正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3 |
D. |
正极为Ag,负极为Fe,电解质溶液为Fe2(SO4)3 |