|
天津是我国研发和生产锂离子电池的重要基地.锂离子电池正极材料是含锂的二氧化钴(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示.电池反应为CoO2+LiC6 | |
| [ ] | |
A. |
充电时,电池的负极反应为LiC6-e- |
B. |
放电时,电池的正极反应为CoO2+Li++e- |
C. |
羧酸、醇等含活泼氢的有机物可用作锂离子电池的电解质 |
D. |
锂离子电池的比能量(单位质量释放的能量)低 |
|
已知2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol,蒸发1 mol H2O(l)需要吸收的能量为44 kJ,其他相关数据如下表:
则表中a为 | |
| [ ] | |
A. |
185.2 |
B. |
224.0 |
C. |
518.8 |
D. |
494. |
|
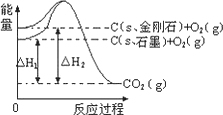
如图所示,ΔH1=-393.5 kJ·mol-1,ΔH2=-395.4 kJ·mol-1,下列说法或表示式正确的是
| |
| [ ] | |
A. |
石墨和金刚石的转化是物理变化 |
B. |
C(s、石墨)=C(s、金刚石) ΔH=+1.9 kJ·mol-1 |
C. |
金刚石的稳定性强于石墨 |
D. |
断裂1 mol石墨的化学键吸收的能量比断裂1 mol金刚石的化学键吸收的能量少 |
|
25℃,101 kPa时,强酸与强碱的稀溶液发生中和反应的中和热为57.3 kJ/mol,辛烷的燃烧热为5518 kJ/mol.下列热化学方程式书写正确的是 | |
| [ ] | |
A. |
2H+(aq)+SO |
B. |
KOH(aq)+ |
C. |
C8H18(l)+ |
D. |
2C8H18(g)+25O2(g)=16CO2(g)+18H2O(l) ΔH=-5518 kJ/mol |
|
下列关于SO2的叙述,正确的是 | |
| [ ] | |
A. |
SO2与水反应生成硫酸 |
B. |
大气中SO2的主要来源是汽车排出的尾气 |
C. |
SO2能漂白某些物质,说明它具有氧化性 |
D. |
SO2既可以是含硫物质的氧化产物,又可以是含硫物质的还原产物 |
|
关于金属腐蚀的叙述中,正确的是 | |
| [ ] | |
A. |
金属被腐蚀的本质是M+nH2O |
B. |
马口铁镀(锡铁)镀层破损后被腐蚀时,首先是镀层被氧化 |
C. |
金属在一般情况下发生的电化学腐蚀主要是吸氧腐蚀 |
D. |
常温下,置于空气中的金属主要发生化学腐蚀 |
|
2011年7月21日,世界各国领导人在南非德班共同商讨应对气候变化的道路——“拯救人类的最后机会”.要想节能减排下列属最有希望的新能源是 ①天然气 ②煤 ③石油 ④水能 ⑤太阳能 ⑥地热能 ⑦风能 ⑧氢能 | |
| [ ] | |
A. |
①②③④ |
B. |
⑤⑥⑦⑧ |
C. |
③④⑤⑥ |
D. |
除①②外 |