|
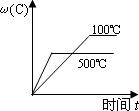
某温度下,在体积一定的密闭容器中进行如下可逆反应: X(g)+Y(g) | |
| [ ] | |
A. |
加入少量W,逆反应速率增大 |
B. |
当容器中气体压强不变时,反应达到平衡 |
C. |
升高温度,平衡逆向移动 |
D. |
平衡后加入X,上述反应的ΔH增大 |
|
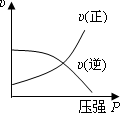
反应A(g)+3B(g) | |
| [ ] | |
A. |
正反应速率加大,逆反应速率变小,平衡向正反应方向移动 |
B. |
正反应速率变小,逆反应速率加大,平衡向逆反应方向移动 |
C. |
正反应速率和逆反应速率变小,平衡向正反应方向移动 |
D. |
正反应速率和逆反应速率变小,平衡向逆反应方向移动 |
|
某温度下的定容密闭容器中,进行如下可逆反应:A(s)+2B(g) ①混合气体的密度 ②容器内气体的压强 ③混合气体的平均相对分子质量 ④B的物质的量浓度 能表明该反应一定已达到平衡状态的是 | |
| [ ] | |
A. |
②③④ |
B. |
②③ |
C. |
①③④ |
D. |
只有④ |
|
一定量的锌粉和6 mol/L的过量盐酸反应,当向其中加入少量的下列物质时,能够加快反应速率,又不影响产生H2的总量的是 ①石墨粉 ②CuO ③铜粉 ④铁粉 ⑤浓盐酸 | |
| [ ] | |
A. |
①②⑤ |
B. |
①③⑤ |
C. |
③④⑤ |
D. |
①③④ |
|
对于反应A(g)+3B(g) | |
| [ ] | |
A. |
v(A)=0.01 mol/(L·s) |
B. |
v(B)=0.02 mol/(L·s) |
C. |
v(B)=0.60 mol/(L·min) |
D. |
v(C)=1.0 mol/(L·min) |
|
已知:①C(s)+ ②C(s)+O2(g) 则反应:C(s)+CO2(g) | |
| [ ] | |
A. |
-283.01 kJ·mol-1 |
B. |
+172.51 kJ·mol-1 |
C. |
+283.01 kJ·mol-1 |
D. |
+504.00 kJ·mol-1 |
|
强酸与强碱的稀溶液发生中和反应:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ/mol,分别向1 L 0.5 mol·L-1的Ba(OH)2的溶液中加入①浓硫酸;②稀盐酸;③稀硝酸,恰好完全反应的热效应分别为ΔH1、ΔH2、ΔH3,下列关系正确的是 | |
| [ ] | |
A. |
ΔH1<ΔH2=ΔH3 |
B. |
ΔH1<ΔH2<ΔH3 |
C. |
ΔH1>ΔH2>ΔH3 |
D. |
ΔH1=ΔH2<ΔH3 |
|
下列热化学方程式中ΔH的值能表示可燃物的燃烧热的是 | |
| [ ] | |
A. |
H2(g)+Cl2(g)=2HCl(g) ΔH=-184.6 kJ/mol |
B. |
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-802.3 kJ/mol |
C. |
2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol |
D. |
CO(g)+1/2O2(g)=CO2(g) ΔH=-283 kJ/mol |