|
X、Y、Z、M代表四种金属元素.金属X和Z用导线连接放入稀硫酸中时,Z极上有H2放出;若电解Y2+和Z2+共存的溶液时,Y先析出;又知M2+的氧化性强于Y2+.则这四种金属的活动性由强到弱的顺序为 | |
| [ ] | |
A. |
X>Z>Y>M |
B. |
X>Y>Z>M |
C. |
M>Z>X>Y |
D. |
X>Z>M>Y |
|
在一定温度下,反应A2(g)+B2(g) | |
| [ ] | |
A. |
单位时间内生成n mol A2的同时生成n mol AB |
B. |
容器内的总物质的量不随时间变化 |
C. |
单位时间内生成2n mol AB的同时生成n mol B2 |
D. |
容器内A2、B2、AB的物质的量之比是1∶1∶2时的状态 |
|
有关如图所示原电池(盐桥中装有含琼胶的KCl饱和溶液)的叙述,正确的是
| |
| [ ] | |
A. |
铜片上有气泡逸出 |
B. |
取出盐桥后,电流计依然发生偏转 |
C. |
反应中,盐桥中的K+会移向CuSO4溶液 |
D. |
反应前后铜片质量不改变 |
|
用纯净的CaCO3与稀HCl反应制CO2,实验过程记录如图所示.根据分析、判断,正确的是
| |
| [ ] | |
A. |
OE段表示的反应速率最快 |
B. |
EF段表示的反应速率最快,收集的CO2最多 |
C. |
FG段收集的CO2最多 |
D. |
OG段表示随着时间的推移,反应速率逐渐增快 |
|
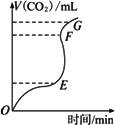
2004年美国圣路易斯大学研制了一种新型的乙醇电池,它用磺酸类质子溶剂,在200℃左右时供电,乙醇电池比甲醇电池效率高出32倍且更安全.电池总反应为: C2H5OH+3O2
| |
| [ ] | |
A. |
a极为电池的负极 |
B. |
电池工作时电流由b极沿导线经灯泡再到a极 |
C. |
电池正极的电极反应为:4H++O2+4e-=2H2O |
D. |
电池工作时,1 mol乙醇被氧化时就有6 mol电子转移 |
|
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是 | |
| [ ] | |
A. |
氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e一=4OH- |
B. |
用铁棒作阳极、碳棒作阴极电解饱和氯化钠溶液的离子方程式为: 2C1-+2H2O |
C. |
粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e-=Cu2+ |
D. |
钢铁发生电化学腐蚀的负极反应式:Fe-2e-=Fe2+ |
|
有关热化学方程式书写与对应表述均正确的是 | |
| [ ] | |
A. |
稀醋酸与0 .1 mol/L NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1 |
B. |
在101 KPa下氢气的标准燃烧热ΔH= -285.5 kJ·mol-1,则水分解的热化学方程式:2H2O(l)=2H2(g)+O2(g) ΔH=+285.5 kJ·mol-1 |
C. |
密闭容器中 ,9.6 g硫粉与11.2 g铁粉混合加热生成硫化亚铁17.6 g时,放出19.12 kJ热量.则Fe(s)+S(s)=FeS(s) ΔH=-95.6 kJ·mol-1 |
D. |
已知 2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1,则可知C的标准燃烧热为110.5 kJ·mol-1 |
|
在密闭容器中发生可逆反应4NH3+5O2 | |
| [ ] | |
A. |
v(O2)=0.01 mol·L-1·s-1 |
B. |
v(NH3)=0.02 mol·L-1·s-1 |
C. |
v(H2O)=0.04 mol·L-1·s-1 |
D. |
v(NO)=0.03 mol·L-1·s-1 |
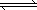 2AB(g)达到平衡状态的标志是
2AB(g)达到平衡状态的标志是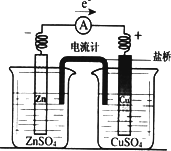
 2CO2+3H2O,电池示意如图,下列说法不正确的是
2CO2+3H2O,电池示意如图,下列说法不正确的是
 4NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是
4NO+6H2O(g),以下是不同情况下的反应速率,其中最快的是