|
用0.1026 mol·L-1的盐酸滴定25.00 mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如下图所示,正确的读数为
| |
| [ ] | |
A. |
22.30 mL |
B. |
22.35 mL |
C. |
23.65 mL |
D. |
23.70 mL |
|
硫代硫酸钠溶液与稀硫酸反应的化学方程式为:Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O四个试管中都装有5 mL 0.1 mol/L Na2S2O3溶液,分别在不同温度下加入0.1 mol/L H2SO4和一定量水,最先出现浑浊的是 | |
| [ ] | |
A. |
20℃,10 mL H2SO4 |
B. |
20℃,5 mL H2SO4,5 mL水 |
C. |
30℃,5 mL H2SO4,2 mL水 |
D. |
30℃,4 mL H2SO4,3 mL水 |
|
已知下列热化学方程式:Zn(s)+1/2O2(g)=ZnO(s) ΔH1=-351.1 kJ/mol Hg(l)+1/2O2(g)=HgO(s) ΔH2=-90.7 kJ/mol.由此可知: Zn(s)+HgO(s)=ZnO(s)+Hg(l) ΔH3.其中ΔH3的值是 | |
| [ ] | |
A. |
-441.8 kJ/mol |
B. |
-254.6 kJ/mol |
C. |
-438.9 kJ/mol |
D. |
-260.4 kJ/mol |
|
原电池是将化学能转化为电能的装置,但其构成具有一定的条件,这些条件是 ①电极(负极与正极:金属活动性不同)、 ②电解质溶液、 ③闭合回路、 ④灯泡 | |
| [ ] | |
A. |
①②③④ |
B. |
①②③ |
C. |
①②④ |
D. |
②③④ |
|
已知4NH3+5O2 | |
| [ ] | |
A. |
4/5v(NH3)=v(O2) |
B. |
5/6v(O2)=v(H2O) |
C. |
4/5v(O2)=v(NO) |
D. |
2/3v(NH3)=v(H2O) |
|
下列电离或化学方程式书写正确的是 | |
| [ ] | |
A. |
Na3PO4=Na++3PO43- |
B. |
CaCO3+2HNO3=Ca(NO3)2+H2O+CO2↑ |
C. |
2KClO3+MnO2 |
D. |
C2H5OH=C2H5O-+H+ |
|
下列反应属于氧化还原反应的是 | |
| [ ] | |
A. |
H2+Cl2 |
B. |
CaCO3+2HCl=CaCl2+CO2↑+H2O |
C. |
CuSO4+BaCl2=BaSO4↓+CuCl2 |
D. |
NH4HCO3 |

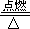 2HCl
2HCl