|
下列洗涤仪器的方法,不可采用的是 | |
| [ ] | |
A. |
盛放过苯酚的试管用NaOH溶液洗涤 |
B. |
盛过油脂的试管用热碱洗涤 |
C. |
沾有硫粉的试管用热的烧碱溶液清洗 |
D. |
用KMnO4分解制备完O2的试管,用稀盐酸洗涤 |
|
下列实验中,金属或固体可以完全溶解的是 | |
| [ ] | |
A. |
在H2O2溶液中加入少量MnO2粉末 |
B. |
表面已经被氧化的铝片加入到足量的NaOH溶液中 |
C. |
1 mol MnO2和含4 mol HCl的盐酸共热 |
D. |
常温下1 mol铁片投入含4 mol HNO3的浓硝酸中 |
|
下列实验操作会引起实验结果偏高的是 | |
| [ ] | |
A. |
测定硫酸铜晶体中结晶水含量的实验中,晶体加热完全失去结晶水后,将盛试样的坩埚放在实验桌上自行冷却 |
B. |
镀锌铁皮锌镀层厚度测量实验中,将铁皮小火烘干、称量时,最后两次称量前后质量不相等 |
C. |
一定浓度的盐酸配制过程中,用量筒量取计算所需的浓盐酸时,仰视观察刻度线 |
D. |
滴定实验时,装待测液的滴定管用蒸馏水洗净后,没有用待测液润洗2~3次 |
|
下列关于实验的叙述正确的是 | |
| [ ] | |
A. |
向一定量的稀硫酸中加入除去油污的稍过量的废铁屑,是制备硫酸亚铁的可行方案 |
B. |
苯酚+碳酸钠→苯酚钠+碳酸氢钠,此反应可说明苯酚的酸性比碳酸强 |
C. |
向铝屑与硫酸反应后的溶液中加入氢氧化钠溶液反应,是制备氢氧化铝的最佳方案 |
D. |
向某溶液中,依次加入氯水和硫氰化钾溶液,溶液变红,说明溶液中含有Fe2+ |
|
下列有关实验操作的说法中正确的是 | |
| [ ] | |
A. |
配制一定物质的量浓度的硫酸溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸馏水洗涤量筒2~3次,并将洗涤液一并倒入烧杯中稀释 |
B. |
用移液管移取溶液时,左手拿洗耳球,右手将移液管插入溶液中吸取 |
C. |
滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面变化 |
D. |
用移液管移取25.00 mL待测液时,若移液管内残留少量液体,应用洗耳球将其吹出,否则使测量结果偏低 |
|
进行下列实验操作时,一般情况下不应该相互接触的是 | |
| [ ] | |
A. |
用移液管移取10 mL NaOH溶液并放于锥形瓶中,移液管的尖嘴和锥形瓶的内壁 |
B. |
分液操作分出下层液体时,分液漏斗下端管口和烧杯的内壁 |
C. |
实验室将HCl气体溶于水时,漏斗口与烧杯内的水面 |
D. |
减压过滤时,布氏漏斗下端管口与吸滤瓶的内壁 |
|
下列结论均出自《实验化学》中的实验,其中不正确的是 | |
| [ ] | |
A. |
硫酸铜溶液中加入过量浓氨水,可得到深蓝色透明溶液 |
B. |
当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 |
C. |
提取海带中碘元素时,为保证I-完全氧化为I2,加入的氧化剂(H2O2或新制氯水)均应过量 |
D. |
制备硫酸亚铁铵晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液表面出现晶膜为止,不能将溶液全部蒸干 |
|
亚硝酸钠的外观与食盐相似,又称“工业食盐”,因此常出现误食工业食盐导致中毒的事件.化学上有许多方法可以用于鉴别食盐和“工业食盐”,下列方法可行的是 ①加入稀硫酸,微热,看能否产生红棕色气体. ②加入酸化的碘化钾淀粉溶液,看溶液是否变蓝. ③加入酸化的氯化亚铁溶液,看溶液是否变成棕黄色. ④加入酸性高锰酸钾溶液,看能否褪色. ⑤加入硝酸酸化的硝酸银溶液,看能否产生白色沉淀. | |
| [ ] | |
A. |
只有①②③④ |
B. |
只有②③④⑤ |
C. |
只有③④⑤ |
D. |
①②③④⑤ |
|
某学生用量筒量取液体,初次视线与量筒内凹液面的最低处保持水平,读数为9.8 mL.倒出部分液体后,俯视凹液面的最低处,读数为3.5 mL,则该学生实际倒出液体的体积 | |
| [ ] | |
A. |
大于6.3 mL |
B. |
小于6.3 mL |
C. |
等于6.3 mL |
D. |
无法确定 |
|
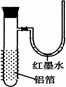
用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升.根据实验现象判断下列说法错误的是
| |
| [ ] | |
A. |
实验中发生的反应都是氧化还原反应 |
B. |
铝是一种较活泼的金属 |
C. |
铝与氧气反应放出大量的热量 |
D. |
铝片上生成的白毛是氧化铝和氧化汞的混合物 |