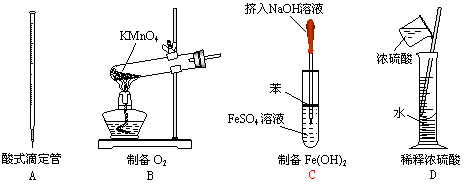
在下列各变化中,反应①为常温下的反应,A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,E常温下为无色无味的液体,F为淡黄色粉末,G为常见的无色气体。

回答下列问题:
(1)A、G的化学式分别为______、______。
(2)A和E反应的离子方程式为______。
(3)写出反应①的化学方程式,并用双线桥法表示出电子转移的情况______。
(4)在反应②中,每生成2.24 L气体G(标准状况)时,该反应转移电子的物质的量是______mol,消耗F______g。
|
特别提示:32小题1班~12班不做,13班、14班必做。 |
下表为元素周期表的一部分。
|
族 周期 |
Ⅰ A |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
1 |
① |
|
|
|
|
|
|
|
2 |
|
|
|
⑥ |
|
⑦ |
⑧ |
|
3 |
② |
④ |
⑤ |
|
|
|
⑨ |
|
4 |
③ |
|
|
|
|
|
⑩ |
请参照元素①—⑩在表中的位置,用化学符号回答下列问题:
(1)元素⑩的电子排布式是______。
(2)在①—⑩中P轨道上有两个未成对电子的元素是______。
(3)在①—⑩中原子半径最大的是______。
(4)②、④、⑤、⑨离子的半径最小的是______。
(5)元素①和⑦的形成化合物和元素⑨的单质发生反应的离子方程式为______。
(6)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为______。
(7)4.6g元素②的单质投入到足量的重水中,则产生的气体中含有______mol中子。
(8)等物质的量的元素⑧的单质和元素②的最高价氧化物对应水化物的恰好完全反应,生成三种产物,产物之一是由两种元素形成的气体化合物,则反应的化学方程式为____________,还原产物是______。
实验室用密度为1.2g/mL,质量分数为36.5%浓盐酸配制250 mL 0.1 mol/L的稀盐酸溶液,填空并请回答下列问题:
(1)列式计算浓盐酸的物质的量浓度:____________________。
(2)配制250mL 0.1mol/L的盐酸溶液
|
应量取浓盐酸体积/mL |
应选用容量瓶的规格/mL |
|
|
|
A.用量筒量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入蒸馏水,用玻璃棒慢慢搅动,使其混合均匀。
B.将已冷却的盐酸沿玻璃棒注入容量瓶中。
C.用蒸馏水洗涤__________2—3次,洗涤液均注入容量瓶,振荡。
D.继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm处,改用__________加水,使溶液凹面恰好与刻度相切。
E.将容量瓶盖紧,振荡,摇匀。
(3)①将烧杯中溶液转移到容量瓶之前,容量瓶中有少量蒸馏水__________(填偏大或偏小或无影响,下同);
②向容量瓶中转移溶液时不慎有液滴掉在容量瓶外面,则浓度__________;
③定容时俯视容量瓶刻度线__________。
 、
、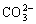 、
、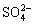 、Cl-、Br-、I-。为了鉴别这些离子,分别取少量溶液进行以下实验:
、Cl-、Br-、I-。为了鉴别这些离子,分别取少量溶液进行以下实验: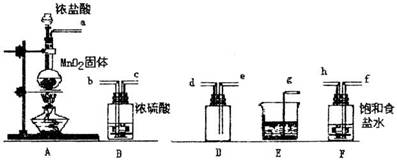
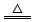 2NH3↑+CO2↑+H2O
2NH3↑+CO2↑+H2O