[s1] 光谱研究表明,易溶于水的S02所形成的溶液中存在着下列平衡:
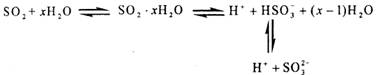
据此,下列判断中正确的是: ( )
A.该溶液中存在着SO2分子 B.该溶液中H+浓度是SO2- 3浓度的2倍
C.向该溶液中加入足量的酸都能放出SO2气体
D.向该溶液中加入过量NaOH可得到Na2SO3 、NaHSO3和NaOH的混合溶液
[s1]14.
[s1] 已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是: ( )
A.该溶液的pH=4 B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
[s1]15.
[s1] 某化学反应中,反应混合物A、B、C的物质的量浓度(c )与时间(t)关系如下所表示:
|
t/ c |
初始 |
2min |
4min |
6min |
8min |
|
c(A)(mol/L) |
1.45 |
1.28 |
1.00 |
1.00 |
1.20 |
|
c(B)(mol/L) |
0.38 |
0.72 |
1.28 |
1.28 |
0.88 |
|
c(C)(mol/L) |
0.095 |
0.18 |
0.32 |
0.32 |
0.42 |
下列说法正确的是: ( )
A.该反应的化学方程式为A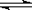 2B+C
B.2 min末A的转化率为11.7%
2B+C
B.2 min末A的转化率为11.7%
C.4--6min时,反应停止了
D.6--8min之间的变化是由于增加了A的浓度引起的
[s1]16.
[s1] 下列叙述正确的是: ( )
A.0.1 mol/LC6H5ONa溶液中:c(Na+)>c(C6H5O-)>c(H+)>c(OH-)
B.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小
C. 在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降
D. pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等
[s1]17.
[s1] 分别取pH均等于2的盐酸和醋酸各l00mL,稀释2倍后,再分别加入足量锌粉,在相同条件下充分反应,下列有关叙述正确的是: ( )
A.反应开始时,盐酸和醋酸分别与锌反应的速率一样大
B. 反应开始时,盐酸与锌反应的速率大
C.盐酸和醋酸分别与锌反应放出的氢气一样多 D.醋酸与锌反应放出氢气多
[s1]18.
[s1] 下列说法不正确的是: ( )
A.电化学腐蚀过程伴随有电流产生,化学腐蚀过程却没有
B.根据氧化还原反应Zn(s)+Fe2+(aq)=Zn2+(aq)+Fe(s)设计一个原电池时,负极是Zn,正极可以是碳棒,电解质溶液是FeCl2
C.氢氧燃料电池中,负极室通入的气体是氧气
D.盐桥是具有导电作用的装置,其作用是将两个半电池连接起来
[s1]19.
[s1] 一定温度下,在氢氧化钡的悬浊液中,存在氢氧化钡固体与其电离的离子间的溶解平衡关系:Ba(OH)2(固体)  Ba2++2OH-。向此种悬浊液中加入少量的氧化钡粉末,下列叙述正确的是:
Ba2++2OH-。向此种悬浊液中加入少量的氧化钡粉末,下列叙述正确的是:
( )
A.溶液中氢氧根离子浓度增大 B.溶液中钡离子浓度减少
 C.溶液中钡离子数目减小
D.pH减小
C.溶液中钡离子数目减小
D.pH减小
[s1]20.
[s1]  用铅蓄电池(总反应:Pb+PbO2+4H++2SO42-
2PbSO4+2H2O)电解苦卤水 (含C1―、Br―、Na+、Mg2+)的装置如图所示 (a、b为石墨电极)。
用铅蓄电池(总反应:Pb+PbO2+4H++2SO42-
2PbSO4+2H2O)电解苦卤水 (含C1―、Br―、Na+、Mg2+)的装置如图所示 (a、b为石墨电极)。
下列说法中正确的是 : ( )
A.铅蓄电池放电时的正极反应是:
PbO2+4H++SO42- =PbSO4+2H2O
B.电解苦卤水时,a 电极首先放电的是Br―而不是Cl―,
说明当其它条件相同时Br―的还原性强于Cl―
C.铅蓄电池充电时,A极应与外接电源负极相连
D.忽略能量消耗,当b极产生0.02g气体时,铅蓄电池中消耗0.01 mol H2SO4
[s1]21.
[s1] 已知25℃、101kpa时,一些物质的燃烧热为:
|
化学式 |
CO(g) |
H2(g) |
CH3OH(l) |
CH4(g) |
|
△H/(kJ/mol)
|
-283.0 |
-285.8 |
-726.5 |
-890.3 |
请回答下列问题。
⑴写出该条件下CH3OH(l)完全燃烧的热化学方程式: 。
⑵根据盖斯定律完成下列反应的热化学方程式:
CO(g)+ 2H2(g)= CH3OH(l);△H= 。
(3)现有H2和CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2(g)和H2O(l),共放出热量3242.5 kJ,则原混合气体中H2和CH4的物质的量之比是:
A.1∶1 B.1∶3 C.1∶4 D.2∶3
[s1]22.
[s1] (1)常温下,有0.1mol/L的盐酸和0.1mol/L的醋酸溶液,回答下列问题:
①比较两溶液的pH ,盐酸 (填“<” 、“=” 或 “>”)醋酸,写出醋酸电离的方程式 。
②两种酸均能与氢氧化钠反应生成盐,其中醋酸与氢氧化钠反应能生成醋酸钠,实验室现有部分醋酸钠固体,取少量溶于水,溶液呈 (填“酸性” 、“中性” 或 “碱性”),其原因是(用离子方程式表示) 。
③向醋酸溶液中加入一定量的NaOH溶液,当测得溶液的pH=7时,溶液中离子的浓度大小为
(填字母,下同),当测得溶液的pH<7时,溶液中离子的浓度大小为 。
a.c(Na+)>c(CH3COO—)>c(OH—)>c(H+) b.c(Na+) = c(CH3COO—)>c(OH—) =c(H+)
c.c(CH3COO—)>c(Na+)>c(H+)>c(OH—) d.c(Na+)>c(CH3COO—)>c(H+)>c(OH—)
(2)向盛有1mL0.1mol/LMgCl2溶液的试管中滴加2滴2mol/L NaOH溶液,有白色沉淀生成,再滴加2滴0.1mol/LFeCl3溶液,静置。可以观察到的现象是 ,产生该现象的原因是(用离子方程式或文字表示) 。
[s1]23.