根据下列结构示意图,判断下列说法中不正确的是( )
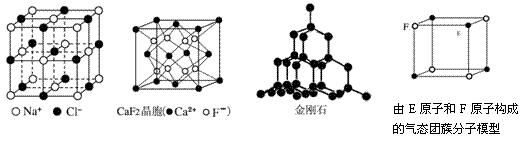 |
A.在NaCl晶体中,距Na+最近的Cl-形成正八面体
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.在金刚石晶体中,碳原子与碳碳键数目比为1:2
D.该气态团簇分子的分子式为EF或FE
根据下列结构示意图,判断下列说法中不正确的是( )
 |
A.在NaCl晶体中,距Na+最近的Cl-形成正八面体
B.在CaF2晶体中,每个晶胞平均占有4个Ca2+
C.在金刚石晶体中,碳原子与碳碳键数目比为1:2
D.该气态团簇分子的分子式为EF或FE