[s1] 将固体FeC2O4·2H2O放在一个可称量的容器中加热灼烧,固体质量随温度升高而变化,测得数据如下:
|
温度/℃ |
25 |
300 |
350 |
400 |
500 |
600 |
900 |
|
固体质量/g |
1.000 |
0.800 |
0.800 |
0.400 |
0.444 |
0.444 |
0.430 |
根据计算分析推理,完成下列填空:
(1)写出25~300℃时固体发生变化的反应方程式 判断的理由是 。
(2)350~400℃发生变化得到的产物是 ,物质的量之比为 。
(3)500℃时产物的含氧质量分数为 。
(4)写出600~900℃时发生变化的化学方程式 。
[s1]30.
[s1] 为检验浓硫酸与木炭在加热条件下反应产生的SO2和CO2气体,设计了如图所示实验装置,a、b、c为止水夹,B是用于储气的气囊,D中放有用I2和淀粉的蓝色溶液浸湿的脱脂棉。
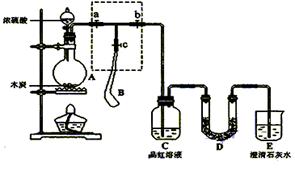
请回答下列问题:
(1)装置A、D中发生反应的化学方程式为 ; 。
(2)实验前欲检查装置A的气密性,可以采取的操作是 ;
(3)此实验成败的关键在于控制反应产生气体的速率不能过快,由此设计了虚框部分的装置,则正确的操作顺序是 (用操作编号填写)
①向A装置中加入浓硫酸,加热,使A中产生的气体进入气囊B,当气囊中充入一定量气体时,停止加热;
②待装置A冷却,且气囊B的体积不再变化后,关闭止水夹a,打开止水夹b,慢慢挤压气囊,使气囊B中气体慢慢进入装置C中,待达到实验目的后,关闭止水夹b;
③打开止水夹a和c,关闭止水夹b;
(4)实验时,装置C中的现象为 ;
(5)当D中产生 (多选不得分)现象时,可以说明使E中澄清石灰水变浑浊的是CO2,而不是SO2;
A.进气口一端脱脂棉蓝色变浅,出气口一端脱脂棉蓝色不变
B.脱脂棉上蓝色均变浅 C.脱脂棉上蓝色褪去
(6)装置D的作用为 。
[s1]31.
[s1] 在由Fe、Fe2O3组成的混合物中加入100mL2mol·L-1的盐酸,恰好使混合物完全溶解,并放出224mL气体(标准状况),经检验溶液中无Fe3+离子,求反应前混合物中Fe、Fe2O3的物质的量。
[s1]32.
[s1] 将5.1 g镁铝合金溶于600 mL 0.5
mol·L-1H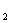 SO
SO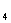 溶液中,完全溶解后再加入1.0 mol·L-1的NaOH溶液,得到沉淀的质量为13.6 g,继续滴加NaOH溶液时则沉淀会减少。
溶液中,完全溶解后再加入1.0 mol·L-1的NaOH溶液,得到沉淀的质量为13.6 g,继续滴加NaOH溶液时则沉淀会减少。
(1)当加入___▲__mLNaOH溶液时,可使溶解在硫酸中的Mg 和Al
和Al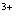 恰好完全沉淀。
恰好完全沉淀。
(2)计算合金溶于硫酸时所产生的氢气在标准状况下的体积。(列出算式)
[s1]33.
 与
与 B、T2O与H2O
C、
B、T2O与H2O
C、 D、金刚石与石墨
D、金刚石与石墨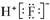
 D、Cl—离子的结构示意图:
D、Cl—离子的结构示意图: 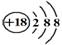
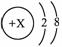 表示某带电微粒的结构示意图,则可用它表示的阳离子共有(
)
表示某带电微粒的结构示意图,则可用它表示的阳离子共有(
)