0 78819 78827 78833 78837 78843 78845 78849 78855 78857 78863 78869 78873 78875 78879 78885 78887 78893 78897 78899 78903 78905 78909 78911 78913 78914 78915 78917 78918 78919 78921 78923 78927 78929 78933 78935 78939 78945 78947 78953 78957 78959 78963 78969 78975 78977 78983 78987 78989 78995 78999 79005 79013 203614
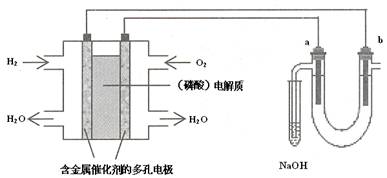
 为直流电源,
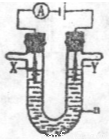
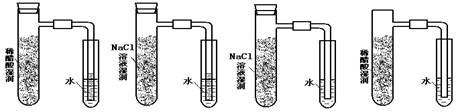
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现 后,使c、d两点短路.下列叙述正确的是( )
后,使c、d两点短路.下列叙述正确的是( )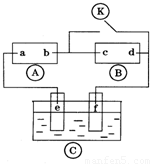
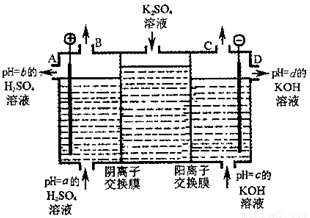
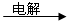 A + B + C
A + B + C

 )+8H2O(
)+8H2O(