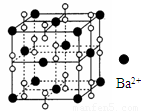
几种短周期元素的原子半径及主要化合价如下表:
|
元素代号 |
L |
M[ |
Q |
R |
T |
|
原子半径/nm[ |
0.160 |
0.143 |
0.102 |
0.089 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
+2 |
-2 |
下列叙述正确的是
A.R的氧化物对应的水化物可能具有两性 B.L、Q形成的简单离子核外电子排布相同
C.T、Q的氢化物的稳定性:Q>T D.L、M的单质中金属键的强弱:L>M
已知晶体硅在氧气中充分燃烧生成1molSiO2晶体可放出989.2 kJ的热量,晶体硅与金刚石结构相似,SiO2晶体的结构如右图,有关键能数据如表:
|
化学键 |
Si—O |
O=O |
Si—Si |
|
键能/kJ·mol-1 |
X |
498.8 |
176 |
则X的值为
A.460 B.920 C.1165.2 D.423.3
(11分) (1)有A、B、C三种晶体,分别由C、H、Na、Cl四种元素中的一种或几种形成,对这三种晶体进行实验,结果见下表。
|
项目 |
熔点/℃[来源:Z。xx。k.Com] |
硬度 |
水溶性 |
导电性 |
水溶液与Ag+反应 |
|
A |
811 |
较大 |
易溶 |
水溶液(或熔融)导电 |
白色沉淀 |
|
B |
3 500 |
很大 |
不溶 |
不导电 |
不反应 |
|
C |
-114.2 |
很小 |
易溶 |
液态不导电 |
白色沉淀 |
① 晶体的化学式及晶体类型分别为:
A________ ____;B_______ ___;C____ ____。
② 晶体中粒子间的作用分别为:
A______ ___;B______ __;C_______ _。
(2)水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。
①写出与H2O分子互为等电子体的微粒__________(填一种即可)。
②水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+)。下列对上述过程的描述不合理的是( )
A.氧原子的杂化类型发生了改变 B.微粒的形状发生了改变
C.微粒的化学性质发生了改变 D.微粒中的键角发生了改变
③下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是______(请用相应的编号填写)