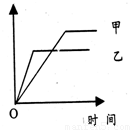
可用下面示意图象表示的是
|
|
反应 |
纵坐标 |
甲 |
乙 |
|
A |
等质量钾、钠分别与水反应 |
H 2质量 |
钠 |
钾 |
|
B |
相同质量氨,在同一容器中 2NH3 |
氨气的转化率 |
500℃ |
400℃ |
|
C |
体积比1:3的N2,H2,在体积可变的恒压容器中,2NH3 |
氨气的浓度 |
活性高的催化剂 |
活性一般的催化剂 |
|
D |
2 mol S02与l mol 02,在相同温度下2S02+02 |
S03物质的量 |
10atm |
2atm |
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净,待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入20.00mL待测溶液到锥形瓶中。
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗2-3次后,向其中注入0.1000 mol·L-1标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于"0"刻度以下的位置,记下读数。
③向锥形瓶中滴入酚酞作指示剂,进行滴定。滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL。
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2 mL。
试回答下列问题:
(1)终点时锥形瓶中的溶液从 色变为 色。
(2)该小组在步骤①中的错误是 ,由此造成的测定
结果 (偏高、偏低或无影响)。
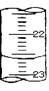
(3)上图,是某次滴定时的滴定管中的液面,其读数为 mL。
(4)根据下列数据:
|
滴定次数 |
待测液体积(mL) |
标准盐酸体积(mL) |
|
|
滴定前读数(mL) |
滴定后读数(mL) |
||
|
第一次 |
20.00 |
0.50 |
25.40 |
|
第二次 |
20.00 |
4.00 |
29.10 |
请计算待测烧碱溶液的浓度为 mol·L-1。
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
|
实验编号 |
HA |
NaOH |
混合溶液的pH |
|
甲 |
[HA]=0.2 mol·L-1 |
[NaOH]=0.2 mol·L-1 |
pH=a |
|
乙 |
[HA]=c1 mol·L-1 |
[NaOH]=0.2 mol·L-1 |
pH=7 |
|
丙 |
[HA]=0.1 mol·L-1 |
[NaOH]=0.1 mol·L-1 |
pH=9 |
|
丁 |
pH=2 |
pH=12 |
pH=b |
请回答:
(1)不考虑其他组的实验结果,单从甲组情况分析,如何用a(混合溶液的pH)来说明HA是强酸还是弱酸?
(2)c1 (填“<”、“>”或“=”)0.2 mol·L-1。乙组实验中HA和NaOH溶液混合前,HA溶液中[A-]与NaOH溶液中[Na+]的关系是 (从下面选项中选择填空)
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是 ,其中,[A-]= mol·L-1(不能做近似计算,回答准确值,结果不一定要化简)。
(4)丁组实验中,HA和NaOH溶液混合前[HA] (填“<”、“>”或“=”)[NaOH], b 7(填“<”、“>”或“=”)
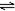 N2+3H2
N2+3H2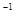 NaOH溶液滴定
20.00mL0.1000 mol·L
NaOH溶液滴定
20.00mL0.1000 mol·L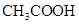 溶液所得滴定曲线如图。下列说法正确的是
溶液所得滴定曲线如图。下列说法正确的是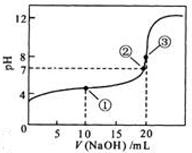
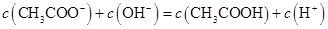
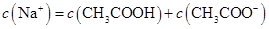
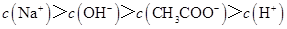
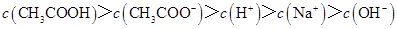
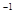 的NaOH溶液中和相同质量的KHC2O4·H2C2O4·2H2O,所需NaOH溶液的体积恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度(mol·L
的NaOH溶液中和相同质量的KHC2O4·H2C2O4·2H2O,所需NaOH溶液的体积恰好为KMnO4溶液的3倍,则KMnO4溶液的浓度(mol·L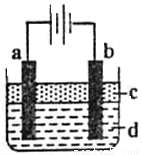
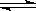 CO2(g)+ H2(g) ;△H<0,在850℃时,平衡常数K=1。
CO2(g)+ H2(g) ;△H<0,在850℃时,平衡常数K=1。