通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键能之和的差。
|
化学键 |
H-H |
Cl-Cl |
H-Cl |
|
生成1mol化学键时放出的能量 |
436kJ |
243kJ |
431kJ |
则下列化学方程式不正确的是
A.1/2H2(g)+1/2Cl2(g)=HCl(g);△H=-91.5kJ·mol-1
B.H2(g)+Cl2(g)=2HCl(g);△H=-183kJ·mol-1
C.1/2H2(g)+1/2Cl2(g)=HCl(g);△H=+91.5kJ·mol-1
D.2HCl(g) =H2(g)+Cl2(g) ;△H=+183kJ·mol-1
当把晶体N2O4放入密闭容器中气化,并建立了N2O4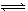 2NO2平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其
2NO2平衡后,保持温度不变,再通入若干N2O4气体,待反应达到新的平衡时,则新平衡与旧平衡相比,其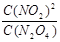 比值
比值
A.变大 B.不变 C.变小 D.无法确定
(15分)下表是稀硫酸与某金属反应的实验数据:
|
实验序号 |
金属 质量/g |
金属状态 |
C(H2SO4) /mol・L-1 |
V(H2SO4) /mL |
溶液温度/℃ |
金属消失的时间/s |
|
|
反应前 |
反应后 |
||||||
|
1 |
0.10 |
丝 |
0.5 |
50 |
20 |
34 |
500 |
|
2 |
0.10 |
粉末 |
0.5 |
50 |
20 |
35 |
50 |
|
3 |
0.10 |
丝 |
0.7 |
50 |
20 |
36 |
250 |
|
4 |
0.10 |
丝 |
0.8 |
50 |
20 |
35 |
200 |
|
5 |
0.10 |
粉末 |
0.8 |
50 |
20 |
36 |
25 |
|
6 |
0.10 |
丝 |
1.0 |
50 |
20 |
35 |
125 |
|
7 |
0.10 |
丝 |
1.0 |
50 |
35 |
50 |
50 |
|
8 |
0.10 |
丝 |
1.1 |
50 |
20 |
34 |
100 |
|
9 |
0.10 |
丝 |
1.1 |
50 |
20 |
44 |
40 |
分析上述数据,回答下列问题:
(1)实验4和5表明: 对反应速率有影响, 反应速率越快,
能表明同一规律的实验还有 (填实验序号);
(2)仅表明反应物浓度对反应速率产生影响的实验有 (填实验序号);
(3)本实验中影响反应速率的其他因素还有 ,其实验序号是 。
(4) 实验中的所有反应,反应前后溶液的温度变化值(约15℃)相近,推测其原因: _________
 Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O cC(g) +dD(g),△H=Q,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示据图分析,以下正确的是
cC(g) +dD(g),△H=Q,反应过程中,当其他条件不变时,某物质在混合物中的含量与温度(T)、压强(p)的关系如图所示据图分析,以下正确的是

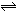 2C(g),2min后反应达到平衡,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是
2C(g),2min后反应达到平衡,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是