(10分)(1)反应Fe(s)+CO2(g) FeO(s)+CO(g) △H1,平衡常数为K1
FeO(s)+CO(g) △H1,平衡常数为K1
反应Fe(s)+H2O(g) FeO(s)+H2(g)
△H2,平衡常数为K2
FeO(s)+H2(g)
△H2,平衡常数为K2
在不同温度时K1、K2的值如下表:
|
|
700℃ |
900℃ |
|
K1 |
1.47 |
2.15 |
|
K2 |
2.38 |
1.67 |
①反应 CO2(g) + H2(g) CO(g) + H2O(g) △H ,平衡常数K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g)
+ H2(g)
CO(g) + H2O(g) △H ,平衡常数K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应CO2(g)
+ H2(g) CO(g) + H2O(g)是
反应(填“吸热”或“放热”)。
CO(g) + H2O(g)是
反应(填“吸热”或“放热”)。
②能判断CO2(g)
+ H2(g) CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)= v逆(H2O) D.c(CO)= c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) FeO(s)+CO(g)
△H > 0,CO2的浓度与时间的关系如图所示:
FeO(s)+CO(g)
△H > 0,CO2的浓度与时间的关系如图所示:
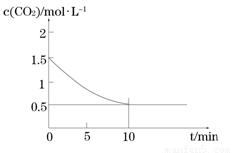
① 该条件下反应的平衡常数为 ;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度 mol·L-1。
②下列措施中能使平衡时 增大的是
(填序号)
增大的是
(填序号)
A.升高温度 B.增大压强
C.充入一定量的CO2 D.再加入一定量铁粉
下表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是
|
元素代号 |
L |
M |
Q |
R |
T |
|
原子半径/nm |
0.160 |
0.134 |
0.089 |
0.102 |
0.074 |
|
主要化合价 |
+2 |
+3 |
+2 |
+6、-2 |
-2 |
A.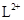 与
与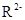 的核外电子数相等
的核外电子数相等
B.L与T形成的化合物具有两性
C.氢化物的稳定性为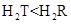 <
<
D.单质与浓度相等的稀盐酸反应的速率为Q<L
 4Fe(OH)3+8OH-+3O2。
4Fe(OH)3+8OH-+3O2。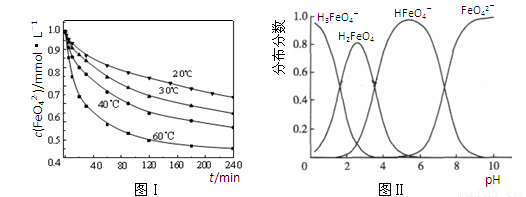

 PCl3(g)+Cl2(g);△H1>0
K1=1mol·L—1
PCl3(g)+Cl2(g);△H1>0
K1=1mol·L—1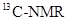 (核磁共振)可用于含碳化合物的结构分析
(核磁共振)可用于含碳化合物的结构分析 N—NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关。
N—NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关。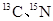 叙述正确的是
叙述正确的是
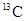 与砖
与砖 N具有相同的中子数 B.
N具有相同的中子数 B. C与
C与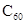 是同一种物质
是同一种物质



 比l mol b从酸中置换
比l mol b从酸中置换 生成的
生成的