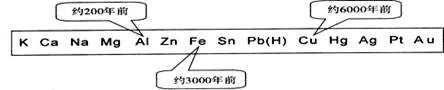
1 L某溶液中含有的离子如下表:
|
离子 |
Cu2+ |
Al3+ |
NO |
Cl- |
|
物质的量浓度(mol/L) |
1 |
1 |
a |
1 |
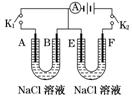
用惰性电极电解该溶液,当电路中有3 mol e-通过时(忽略电解时溶液体积的变化及电极产物可能存在的溶解现象),下列说法正确的是
A.a=3 B.电解后溶液的c(H+)=1mol·L-1
C.电解该溶液相当于只电解CuCl2溶液 D.阴极析出的金属是铜与铝
如图所示,隔板I固定不动,活塞Ⅱ可自由移动,M、N两个容器中均发生反应:A(g) + 2B(g) xC(g)ΔH=-192kJ·mol-1。向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
xC(g)ΔH=-192kJ·mol-1。向M、N中都通入1molA和2molB的混合气体,初始M、N容积相同,保持温度不变。下列说法正确的是
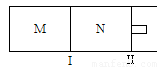
A.若x=3,达到平衡后A的体积分数关系为:φ(M)>φ(N)
B.若x>3,达到平衡后B的转化率关系为:α(M)>α(N)
C.若x<3,C的平衡浓度关系为:c(M)>c(N)
D.x不论为何值,起始时向N容器中充入任意值的C,平衡后N容器中A的浓度均相等
(14分)二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。请回答下列问题:
⑴ 煤的气化的主要化学反应方程式为:___________________________。
⑵ 利用水煤气合成二甲醚的三步反应如下:
① 2H2(g)
+ CO(g) CH3OH(g)
ΔH=-90.8 kJ·mol-1 K1
CH3OH(g)
ΔH=-90.8 kJ·mol-1 K1
② 2CH3OH(g) CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1 K2
CH3OCH3(g) + H2O(g);ΔH=-23.5 kJ·mol-1 K2
③ CO(g) + H2O(g) CO2(g)
+ H2(g);ΔH=-41.3 kJ·mol-1 K3
CO2(g)
+ H2(g);ΔH=-41.3 kJ·mol-1 K3
总反应:3H2(g) +
3CO(g) CH3OCH3(g) +CO2 (g)的ΔH= _____ , K=
(用包含K1、 K2、 K3的式子表示).一定条件下的等容密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是
(填字母代号)。
CH3OCH3(g) +CO2 (g)的ΔH= _____ , K=
(用包含K1、 K2、 K3的式子表示).一定条件下的等容密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是
(填字母代号)。
a.高温高压 b.加入催化剂 c减少CO2的浓度
d.增加CO的浓度 e.增加H2的浓度 f.充入He
(3)已知反应②2CH3OH(g)
 CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g) + H2O(g)某温度下的平衡常数为400 。此温度下,在密闭容器中加入CH3OH ,反应到某时刻测得各组分的浓度如下:
|
物质 |
CH3OH |
CH3OCH3 |
H2O |
|
浓度/(mol·L-1) |
0.44 |
0.6 |
0.6 |
① 比较此时正、逆反应速率的大小:v(正) ______ v(逆) (填“>”、“<”或“=”)。
② 若加入CH3OH后,经10 min反应达到平衡,此时c(CH3OH) = _________,该时间内反应速率v(CH3OH) = __________。
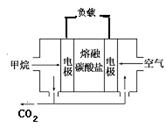
(14分)美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如下图:
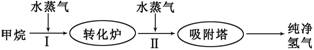
(1)此流程的第II步反应为:CO(g)+H2O(g) H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
H2(g)+CO2(g),该反应的平衡常数随温度的变化如下表:
|
温度/℃ |
400 |
500 |
830 |
|
平衡常数K |
10 |
9 |
1 |
从上表可以推断:此反应是 (填“吸”或“放”)热反应。在830℃下,若开始时向恒容密闭容器中充入1mo1CO和2mo1H2O,则达到平衡后CO的转化率为 。
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第II步反应,达到平衡后下列关系正确的是
|
实验编号 |
反应物投入量 |
平衡时H2浓度 |
吸收或放出的热量 |
反应物转化率 |
|
A |
1、1、0、0 |
c1 |
Q1 |
α1[来源:] |
|
B |
0、0、2、2 |
c2 |
Q2 |
α2
|
|
C |
2、2、0、0 |
c3 |
Q3 |
α3 |
A.2c1= c2 =c3 B.2Q1=Q2=Q3 C.α1 =α2 =α3 D.α1 +α2 =1
(3)在一个绝热等容容器中,不能判断此流程的第II步反应达到平衡的是 。
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化 ⑥v(CO2)正=v(H2O)逆
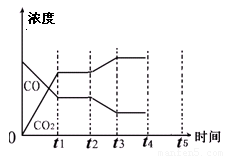
(4)下图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是 、
(写出两种)。若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变)。
 PCl3(g)+Cl2(g) ②2HI(g)
PCl3(g)+Cl2(g) ②2HI(g)
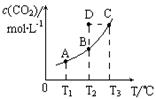
 CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如图所示。下列说法错误的是