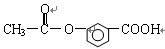
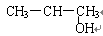有四组同族元素的物质,在101.3 kPa时测定它们的沸点(℃)如下表所示:
|
第一组 |
He -268.8 |
(a) -249.5 |
Ar -185.8 |
Kr -151.7 |
|
第二组 |
F2 -187.0 |
Cl2 -33.6 |
(b) 58.7 |
I2 184.0 |
|
第三组 |
(c) 19.4 |
HCl -84.0 |
HBr -67.0 |
HI -35.3 |
|
第四组 |
H2O 100.0 |
H2S -60.2 |
H2Se -42.0 |
H2Te -1.8 |
下列各项中正确的是
A.a、b、c的化学式分别为Ne2、Br2、HF
B.第二组物质只表现氧化性,不表现还原性
C.第三组物质中C的沸点最高,是因为C分子内存在氢键
D.第四组中各化合物的稳定性顺序为:H2O>H2S> H2Se>H2Te
有机物在反应中,常有下列原子间的共价键全部或部分断裂,如C—H、C—C、C=C、C—O、C═O等。下列各反应中,反应物分子中断裂键的排列,正确的组合是
|
化学反应 |
乙醇酯化 |
乙醇氧化 |
丙烷取代 |
乙酸酯化 |
丙烯加成 |
|
A |
O—H |
C—H |
C—H |
C—O |
C=C |
|
B |
O—H |
O—H |
C—C |
C═O |
C—H |
|
C |
C—O |
C—O |
C—H |
O—H |
C—C |
|
D |
C—O |
C—H |
C—C |
C—O |
C=C |
 2 NO(g)已达到平衡状态的标志的是
2 NO(g)已达到平衡状态的标志的是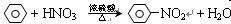 ; 取代反应
; 取代反应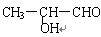 D.
D.