已知H2(g)+Br2(l)=2HBr(g);△H=-72KJ/mol,蒸发1molBr2(l)需要吸收的能量为30KJ,其他的相关数据如下表:
|
|
H2(g) |
Br2(g) |
HBr(g) |
|
1mol分子中的化学键断裂时需要吸收的能量/kJ |
436 |
a |
369 |
则表中a为
A.404 B. 260 C.230 D.200
硫代硫酸钠溶液与稀硫酸反应的化学方程式为: Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O,下列各组实验中最先出现浑浊的是
|
实验 |
反应温度/℃ |
Na2S2O3溶液 |
稀H2SO4 |
H2O |
||
|
V/mL |
c/(mol·L-1) |
V/mL |
c/(mol·L-1) |
V/mL |
||
|
A |
25 |
5 |
0.1 |
10 |
0.1 |
5 |
|
B |
25 |
5 |
0.2 |
5 |
0.2 |
10 |
|
C |
35 |
5 |
0.1 |
10 |
0.1 |
5 |
|
D |
35 |
5 |
0.2 |
5 |
0.2 |
10 |
I2在KI溶液中存在下列平衡:I2(aq)+I-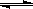 I3-(aq)。测得不同温度下该反应的平衡常数K如下表:
I3-(aq)。测得不同温度下该反应的平衡常数K如下表:
|
t/℃ |
5 |
15 |
25 |
35 |
50 |
|
K |
1100 |
841 |
680 |
533 |
409 |
下列说法正确的是
A.反应I2(aq)+I-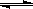 I3-(aq)的ΔH>0
I3-(aq)的ΔH>0
B.其他条件不变,升高温度,溶液中c(I3-)减小
C.该反应的平衡常数表达式是K=c(I2)·c(I-)/c(I3-)
D.25℃时,向溶液中加入少量KI固体,平衡常数K小于680
 C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是