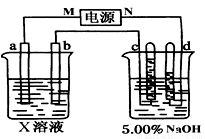
(6分)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)终点的判断:溶液由_____________________________________________________。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是( )
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则所用
盐酸溶液的体积为_________ml。

(4)某学生根据3次实验分别记录有关数据如表:
|
滴定 次数 |
待测NaOH溶液的体积/mL |
0.1000 mol/L盐酸的体积/mL |
||
|
滴定前刻度 |
滴定后刻度 |
平均耗用盐酸 体积/mL |
||
|
第一次 |
25.00 |
0.00 |
26.15 |
①V=__________ |
|
第二次 |
25.00 |
0.56 |
30.30 |
|
|
第三次 |
25.00 |
0.20 |
26.45 |
②依据上表数据列式计算该NaOH溶液的物质的量浓度(计算结果取4位有效数)。
(8分)室温下,将1.00mol/L盐酸滴入20.00mL 1.00mol/L氨水中,溶液pH和温度(0C)
随加入盐酸体积变化曲线如右图所示。

(1)下列有关说法正确的是___________
A.a点由水电离出的C(H+)=10-14mol/L
B.b点:
C.c点:C(Cl-)=C(NH4+)
D.d点后,容易温度略下降的主要原因是NH3·H2O电离吸热
(2)在滴加过程中,水的电离程度的变化是先 后 (填“增大”、“减小”或“不变”);
(3)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和
溶液的pH。试填写表中空白:
|
|
离子浓度的关系 |
溶质 |
溶液的pH |
物料守恒关系 |
|
① |
C(NH4+)>C(Cl-)>C(OH-)>C(H+) |
|
pH>7 |
/ |
|
② |
|
NH4Cl |
/ |
|
|
③ |
C(Cl-)>C(H+)>C(NH4+)>C(OH-) |
|
pH<7 |
/ |


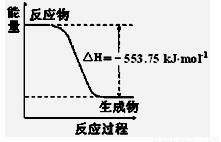
 2NH3(g);△H<0 。
2NH3(g);△H<0 。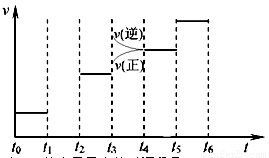
 2SO3(g);
2SO3(g);