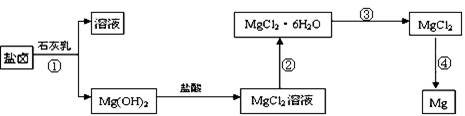
(13分)合成氨工业对国民经济和社会发展具有重要的意义。其原理为:
N2(g)+3H2(g)  2NH3(g) △H= -92.4 kJ/mol 据此回答以下问题:
2NH3(g) △H= -92.4 kJ/mol 据此回答以下问题:
(1)合成氨工业采取的下列措施中,不能用勒沙特列原理解释的是 (填序号)。
①反应压强为20Mpa~50Mpa ②500℃的高温 ③铁触媒作催化剂 ④将生成的氨液化并及时从体系中分离出来,未反应的N2、H2循环到合成塔中。
(2)一定条件下NH3的平衡体积分数随n(N2)变化如图所示(T-温度)。则T2 T1(填>、=、<),判断的依据是:

(3)合成氨气所需的氢气可以由水煤气分离得到。涉及反应信息如下:
反应一:C(s)+H2O(g)  H2(g)+CO(g)
平衡常数K1
H2(g)+CO(g)
平衡常数K1
反应二:CO(g)+H2O(g)  H2(g)+CO2(g) 平衡常数K2
H2(g)+CO2(g) 平衡常数K2
① K1的表达式:K1=
②将一定量的H2O(g)和CO(g)分别通入到体积为1L的密闭容器中,在不同条件下进行反应,得到以下三组数据:
|
实验组别 |
温度/℃ |
起始量/mol |
平衡量/mol |
达到平衡所需时间/min |
||
|
H2O |
CO |
H2 |
CO |
|||
|
1 |
650 |
1 |
2 |
0.8 |
1.2 |
5 |
|
2 |
900 |
0.5 |
1 |
0.2 |
0.8 |
3 |
|
3 |
T |
a |
b |
c |
d |
t |
(Ⅰ)实验1中,用CO2表示反应开始到平衡的平均反应速率为
(Ⅱ) 在实验3,当a=0.5、b=1时,要使c、d数据与实验2相同,且t<3,可以采取的措施为 (填序号)
A.其它条件不变温度T<900℃ B.其它条件不变温度T>900℃
C.充入一定量氖气 D.使用高效催化剂
(Ⅲ)对于反应二,当升高温度时K2 (填“增大”、“减小”或“不变”)。
(8分)微生物燃料电池(MFC)是燃料电池中特殊的一类,它利用微生物作为反应主体,将有机物的化学能转化为电能。以葡萄糖溶液作底物为例,其工作原理如图所示。
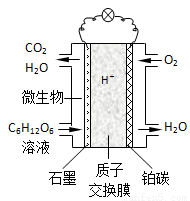
已知石墨电极上反应为:
C6H12O6+6H2O-24e-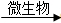 6CO2+24H+
6CO2+24H+
⑴ 电池中的质子交换膜只允许质子和水分子通过。电池工作时质子移向电源的 极
铂碳上所发生的电极反应式为_____________。
⑵燃烧热是指1摩尔物质完全燃烧生成稳定的物质(如H转化为液态水,C转化为二氧化碳 )所放出的热量。葡萄糖的燃烧热为2800kJ/mol,写出葡萄糖燃烧的热化学方程式 。
⑶ 化学需氧量(COD)是重要的水质指标,其数值表示将1L水中的有机物氧化为CO2、H2O所需消耗的氧气的质量。科学家设想利用微生物燃料电池来处理某些污水,并进行发电,该设想已经在实验室中获得成功。但如果1L废水中有机物(折算成葡萄糖)氧化提供的化学能低于5.6kJ,就没有发电的必要。则下列污水中,不适合用微生物燃料电池发电的是 (填序号)。
|
序号 |
A |
B |
C |
D |
E |
|
污水类型 |
生活污水 |
印染 |
电镀 |
造纸 |
硫酸工业废水 |
|
COD值(mg/L) |
520 |
870 |
20 |
960 |
120 |
(11分)某学生用0.2000mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作可分为如下几步: ①用蒸馏水洗涤碱式滴定管,注入0.2000mol·L-1的标准NaOH溶液至“0”刻度线以上
②固定好滴定管并使滴定管尖嘴充满液体;
③调节液面至“0”或“0”刻度线稍下,并记下读数;
④量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
⑥重复以上滴定操作2-3次。
请回答:
(1)以上步骤有错误的是(填编号)________,该错误操作会导致测定结果_________
(填“偏大”、“偏小”或“无影响”)。
(2)步骤④中,量取20.00mL待测液应使用__________________(填仪器名称),在锥形瓶装液前,留有少量蒸馏水,测定结果____________(填“大”、“偏小”或“无影响”)。
(3)步骤⑤滴定时眼睛应注视 _______________________________判断到达滴定终点的依据是:__________________________________________________。
(4)以下是实验数据记录表
|
滴定次数 |
盐酸体积(mL) |
NaOH溶液体积读数(mL) |
|
|
滴定前 |
滴定后 |
||
|
1 |
20.00 |
0.00 |
18.10 |
|
2 |
20.00 |
0.00 |
16.30 |
|
3 |
20.00 |
0.00 |
16.22 |
从上表可以看出,第1次滴定记录的NaOH溶液体积明显多于后两次的体积,其可能的原因是( )
A.滴定前滴定管尖嘴有气泡,滴定结束无气泡
B.锥形瓶用待测液润洗
C.NaOH标准液保存时间过长,有部分变质
D.滴定结束时,俯视计数
(5) 根据上表记录数据,通过计算可得,该盐酸浓度为:____________mol·L-1
 2E(g),若开始时只充入2 mol E气体,达到平衡时,混合气体的压强比起始增大了20%;若开始时只充入了3 mol
M和1 mol N的混合气体,达到平衡时M的转化率为( )
2E(g),若开始时只充入2 mol E气体,达到平衡时,混合气体的压强比起始增大了20%;若开始时只充入了3 mol
M和1 mol N的混合气体,达到平衡时M的转化率为( )
 Si(s)+4HCl(g);
ΔH=+QkJ/mol(Q>0),下列叙述正确的是 (
)
Si(s)+4HCl(g);
ΔH=+QkJ/mol(Q>0),下列叙述正确的是 (
)