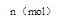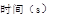四个体积相同的密闭容器中在一定的条件下发生反应:2SO2+O2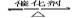 2SO3,反应开始时,反应速率由大到小排列顺序正确的是( )
2SO3,反应开始时,反应速率由大到小排列顺序正确的是( )
|
容器 |
温度 |
SO2(mol) |
O2(mol) |
催化剂 |
|
甲 |
5000C |
10 |
5 |
- |
|
乙 |
5000C |
8 |
5 |
V2O5 |
|
丙 |
4500C |
8 |
5 |
- |
|
丁 |
5000C |
8 |
5 |
- |
A.乙>甲>丁>丙 B.乙>甲>丙>丁 C.甲>乙=丁>丙 D.乙>甲>丙=丁
(12分)电解原理在化学工业中有广泛应用。右图表示一个电解池,其中a为电解质溶液, X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:(1)X的电极名称是 (填写“阳极”或“阴极”)。

(2)若X、Y都是惰性电极,a是饱和食盐水,实验开始时,
同时在两边各滴入几滴酚酞试液,一段时间后,在X极附近
观察到的现象是 ,Y极上的电极反应为 。
(3)若X、Y都是惰性电极,a是CuSO4溶液,电解一段时间后,阳极上产生气体的体积为0.224L(标准状况下),则阴极上析出金属的质量为 g。
(4)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是 ,Y电极的材料是 。
(5)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是 。
|
方案 |
X |
Y |
a溶液 |
|
A |
银 |
石墨 |
AgNO3 |
|
B |
银 |
铁 |
AgNO3 |
|
C |
铁 |
银 |
Fe(NO3)3 |
|
D |
铁 |
银 |
AgNO3 |
(14分)在80℃时,0.40mol的N2O4气体充入2L固定容积的密闭容器中发生如下反应:N2O4(g)
 2 NO2(g) ΔH>0 ,隔一段时间对该容器内的物质进行分析得到如下数据:
2 NO2(g) ΔH>0 ,隔一段时间对该容器内的物质进行分析得到如下数据:
|
|
0 |
20 |
40 |
60 |
80 |
100 |
|
n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
|
n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
(1)求b、e的值:b= ,e=
(2)20s—40s内用N2O4表示的平均反应速率为 _;80℃该反应的化学平衡常数K为 __。
(3)改变条件达到新平衡,要使NO2在平衡体系中体积分数变小,采取的措施有 。A.向混合气体中再通入N2O4 B.保持容积不变,通入He C.使用高效催化剂 D.降低温度
(4) 如果在80℃、将0.40mol的N2O4气体放入一个起始体积为2L、且压强维持不变的容器中发生上述反应。则达到平衡时n(NO2) 0.60mol(填“ 大于 ” “等于” 或“ 小于”)
(5)如图是80℃时容器中N2O4物质的量的变化曲线,请在
该图中补画出该反应在60℃时N2O4物质的量的变化曲线