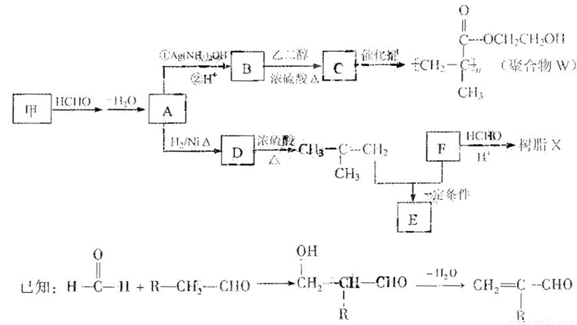
(14 分)
根据要求完成下列各小题实验目的。(a、b为弹簧夹,加热及固定装置已略去)
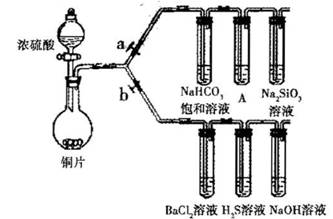
(1)验证碳、硅非金属性的相对强弱。(巳知酸性:亚硫酸 >碳酸)
①连接仪器. ________、加药品后,打开a关闭 b,然后滴入滚硫酸,加热
②铜与浓硫酸反应的化学方程式是________________装置A屮的试剂是________
③能说明碳的非金属性比硅强的实验现象是:________
(2)验证 SO,的氧化性.、还原性和酸性氧化物的通性。
①打开b,关闭a。
②H2S溶液中宥浅黄色浑浊出现,化学方程式是:_____
③BaCl2溶液中无叨诚现象,将其分成两份,分別滴加下列溶液,将产生的沉淀的化学式填人下表相应位置
|
滴加的溶液 |
氯水 |
氨水 |
|
沉淀的化学式 |
|
|
写出其中SO2 显示还原性并生成沉淀的离子方程式_________
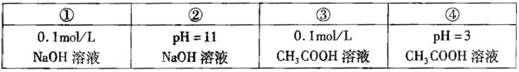
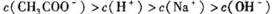

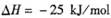 ,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加人CH3OH,反应到某时刻测得各组分的物质的量浓度如下:
,某温度下的平衡常数为400。此温度下,在1 L的密闭容器中加人CH3OH,反应到某时刻测得各组分的物质的量浓度如下:

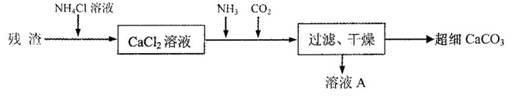
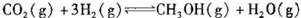 .
.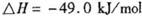 O
O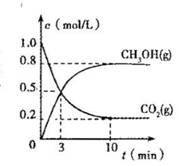



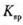 越小,表示该物质在水中越易沉淀)
越小,表示该物质在水中越易沉淀)