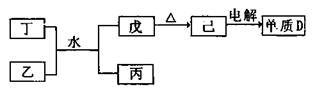
某无色溶液中含有:①Na+、②Ba2+、③Cl-、④Br-、⑤SO2-3、⑥SO2-4-离子中的一种或几种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
|
步骤 |
操作 |
现象 |
|
① |
用pH试纸检验 |
溶液的pH大于7 |
|
② |
向溶液中滴加氯水,再加入CCl4振荡,静置 |
CCl4层呈橙红色 |
|
③ |
取②的上层溶液,加入Ba(NO3)2溶液和稀HNO3 |
有白色沉淀产生 |
|
④ |
将③过滤,向滤液中加入AgNO3溶液和稀HNO3 |
有白色沉淀产生 |
根据上述实验现象,判断以下结论中正确的是
A.肯定含有的离子是①④⑤ B.肯定没有的离子是②⑤
C.可能含有的离子是①②⑥ D.不能确定的离子是①③⑥
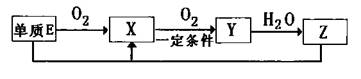
(16分)工业合成氨与制备硝酸一般可连续生产,流程如下:

(1)工业生产时,制取氢气的一个反应为:CO+H2O(g) CO2+H2。t℃时,往1L密闭容器中充入0.2mol
CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K= (填计算结果)。
CO2+H2。t℃时,往1L密闭容器中充入0.2mol
CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K= (填计算结果)。
(2)合成培中发生反应N2(g)+3H2(g) 2NH3(g)△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1
300℃(填“>”、“<”或“=”)。
2NH3(g)△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中T1
300℃(填“>”、“<”或“=”)。
|
T/℃ |
T1 |
300 |
T2 |
|
K |
1.00×107 |
2.45×105 |
1.88×103 |
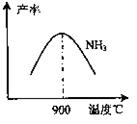
(3) N2和H2在铁作催化剂作用下从145℃就开始反应,不同温度下NH3产率如图所示。温度高于900℃时,NH3产率下降的原因 。
(4)在上述流程图中,氧化炉中发生反应的化学方程式为 。
(5)硝酸厂的尾气含有氮的氧化物,如果不经处理直接排放将污染空气。目前科学家探索利用燃料气体中的甲烷等将氮的氧化物还原为氮气和水,反应机理为:
CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g)△H= -574kJ·mol-1
CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) △H= -1160kJ·mol-1
则甲烷直接将N02还原为N2的热化学方程式为: 。
(6)氨气在纯氧中燃烧,生成一种单质和水,试写出该反应的化学方程式 ,科学家利用此原理,设计成氨气一氧气燃料电池,则通入氨气的电极是 (填“正极”或“负极”);碱性条件下,该电极发生反应的电极反应式为 。
(14分)我国制碱工业的先驱——侯德榜先生,1939年发明了著名的侯氏制碱法,其核心反应原理可用如下化学方程式表示:
NH3+CO2+NaCl+H2O===NH4Cl+NaHCO3(晶体),
依据此原理,欲制得碳酸氢钠晶体,某校学生设计了如下实验装置,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和。
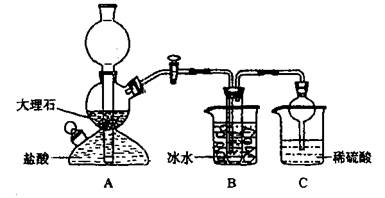
(1)A装置中所发生反应的离子方程式为 。
C装置中稀硫酸的作用为 。
(2)下表中所列出的是相关物质在不同温度下的溶解度数据(g/100g水)
|
温度 溶解度 盐 |
0℃ |
10℃ |
20℃ |
30℃ |
40℃ |
50℃ |
|
NaCl |
35.7 |
35.8 |
36.0 |
36.3 |
36.6 |
37.0 |
|
NaHCO3 |
6.9 |
8.1 |
9.6 |
11.1 |
12.7 |
14.5 |
|
NH4Cl |
29.4 |
33.3 |
37.2 |
41.4 |
45.8 |
50.4 |
参照表中数据,请分析B装置中使用冰水的目的是 。
(3)该校学生在检查完此套装置气密性后进行实验,结果没有得到碳酸氢钠晶体,指寻教师指出应在 装置之间(填写字母)连接一个盛有 的洗气装置,其作用是 。
(4)若该校学生进行实验时,所用饱和食盐水中含NaCl的质量为5.85g,实验后得到干燥的NaHCO3晶体的质量为5.04g,则NaHCO3的产率为 。


 N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态
N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态