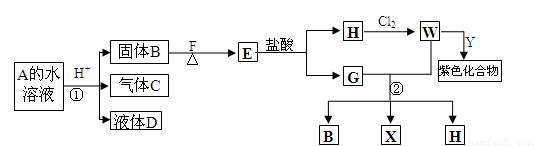
下表中的实验操作能达至实验目的或得出相应结论的是 ( )
|
选项 |
实验操作 |
实验目的或结论 |
|
A |
某实验得到热化学方程式: S(l)+O2(g)=SO2(g);ΔH=-293.23kJ/mol |
1molSO2的键能的总和小于1mol硫和1mol氧气的键能之和 |
|
B |
C2H5Br与NaOH溶液混合充分振荡,再加入AgNO3溶液 |
检验C2H5Br中的溴元素 |
|
C |
向某溶液中加入2滴KSCN溶液,溶液不显红色;再向溶液中加入几滴新制的氯水,溶液变为红色 |
说明溶液中一定含有Fe2+ |
|
D |
将少量某物质滴加到新制的氢氧化铜悬浊液中,加热后有红色沉淀生成 |
说明该物质一定是醛 |
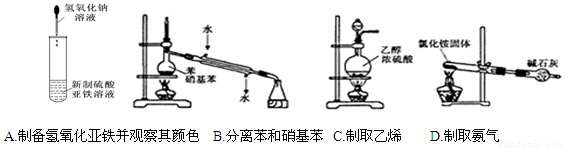

 K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是( )
K2S4+3KI。装置(II)为电解池的示意图。当闭合开关K时,电极X附近溶液先变红。则闭合K时,下列说法正确的是( )
 2NH3(g)的△H= ▲ 。
2NH3(g)的△H= ▲ 。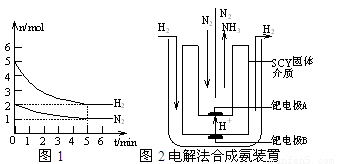
 CO(g)+3H2(g) ΔH1
CO(g)+3H2(g) ΔH1