(16分)已知某酸性土壤浸取液中除Fe3+外,还含有一定量Mg2+和Al3+。请设计合理实验检验该浸取液中的Mg2+、Al3+。
限选实验用品与试剂:烧杯、试管、玻璃棒、滴管、玻璃片、pH试纸;浸取液、20%KSCN、0.1 mol·L-1NaOH、6 mol·L-1NaOH、0.1 mol·L-1HCl、蒸馏水。
必要时可参考:
|
沉淀物 |
开始沉淀时的pH |
沉淀完全时的pH |
|
Mg(OH)2 |
9.6 |
11.1 |
|
Fe(OH)3 |
2.7 |
3.7 |
根据你设计的实验方案,叙述实验操作、预期现象和结论。(测定溶液pH的具体操作可不写)
|
实验操作 |
预期现象和结论 |
|
步骤1: |
|
|
步骤2: |
|
|
步骤3: |
|
|
…… |
|
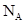 表示阿伏伽德罗常数,下列判断正确的是
表示阿伏伽德罗常数,下列判断正确的是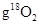 中含有
中含有
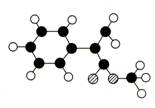
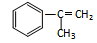 出发来合成M,其合成路线如下:
出发来合成M,其合成路线如下: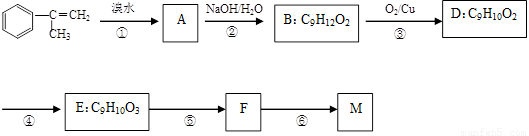
 H2+I2
H2+I2

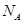 表示阿伏加德罗常数,下列说法正确的是 ( )
表示阿伏加德罗常数,下列说法正确的是 ( )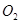 共转移
共转移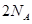 个电子
个电子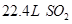 气体的质量大致相等
气体的质量大致相等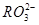 离子的质量为40g,则
离子的质量为40g,则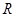 的摩尔质量为32g·mol–1
的摩尔质量为32g·mol–1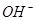 )离子
)离子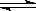 2NH3,3秒钟后,NH3的物质的量增加0.12mol,用H2浓度的变化表示3秒钟内的平均反应速率为 ( )
2NH3,3秒钟后,NH3的物质的量增加0.12mol,用H2浓度的变化表示3秒钟内的平均反应速率为 ( )