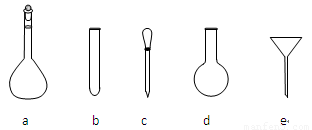
(8分)某研究性学习小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO2气体中燃烧。他们对钠在CO2气体中燃烧后的产物中的白色物质进行了如下探究:
【实验】将燃烧的钠迅速伸入到盛有装满CO2的集气瓶中,钠在其中继续燃烧,反应后冷却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
【提出假设】
假设1:白色物质是Na2O。
假设2:白色物质是Na2CO3。
假设3:白色物质是Na2O和Na2CO3的混合物。
【设计实验方案.验证假设】该小组对燃烧后的白色产物进行如下探究:
|
实验方案 |
实验操作 |
实验现象 |
结论 |
|
方案1 |
取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 |
溶液变成红色 |
白色物质为Na2O |
|
方案2 |
①取少量白色物质于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的CaCl2溶液 |
出现白色沉淀 |
|
|
③静置片刻,取上层清液于试管中,滴加无色酚酞试液 |
无明显现象 |
【思考与交流】
(1)甲同学认为方案1得到的结论不正确,其理由是 。
(2)乙同学认为方案2得到的结论正确,白色物质为 。
(3)通过方案1和方案2的实验,你认为上述三个假设中, 成立。你的理由是 。
(4)钠在二氧化碳中燃烧的化学方程式为 。
(5)丙同学认为白色物质有可能是氢氧化钠。你是否同意丙同学的观点,并简述理由: 。
(12分)下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
|
|
② |
④ |
|
|
3 |
⑤ |
|
③ |
|
|
⑥ |
⑦ |
|
(1)④、⑤、⑦的原子半径由大到小的顺序为___________。
(2)⑥和⑦的最高价含氧酸的酸性强弱为__ ___>_______。
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为__________。在酸性溶液中该物质能将Fe2+氧化,写出该反应的离子方程式____________。
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体,D溶液显碱性。

① 写出D溶液与G反应的化学方程式____________。
② 写出检验A溶液中溶质的阴离子的方法: ____________。
③ 常温下,若电解1 L 0.1 mol/L A溶液,一段时间 后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为__________ mol。
④ 若上图中各步反应均为完全转化,则混合物X中含有的物质有_______。
(8分)现有A、B、C、D、E五种可溶强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
|
阳离子 |
H+、Na+、Al3+、Ag+、Ba2+ |
|
阴离子 |
OH—、Cl—、CO32—、NO3—、SO42— |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②向E溶液中逐滴滴加B溶液至过量,沉淀量先增加后减少但不消失。
③D溶液与另外四种溶液反应都能产生沉淀。
试回答下列问题:
(1)A溶液呈碱性的原因是 。
(2)写出E溶液与过量的B溶液反应的离子方程式 。
(3)已知:NaOH(aq)+HNO3(aq)=NaNO3(aq)+H2O(1);△H= —a kJ·mol-1。
请写出相同条件下B与C的稀溶液反应的热化学方程式 。
(4)若25°时C、E溶液pH=4,则E溶液中水电离出的氢离子浓度是C溶液中水电离出的氢离子浓度 倍。
(5)将C溶液逐滴加入等体积、等物质的量的浓度的A溶液中,反应后溶液中一价离子(+1或一1)浓度由大到小的顺序为: 。


 SO32-+H3O+
SO32-+H3O+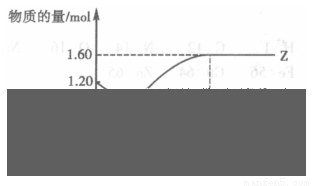
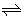 2Z(g),平衡常数K=40
2Z(g),平衡常数K=40 (
( 