为了研究在温度对苯催化加氢的影响,以检验新型镍催化剂的性能。采用相同的微型反应装置,压强为0.78Mpa,氢气、苯的物质的量之比为6.5:1。定时取样分离出氢气后,分析成分得如下表结果:
|
温度/℃ |
85 |
95 |
100 |
110~240 |
280 |
300 |
340 |
|
|
质量分数(%) |
苯 |
96.05 |
91.55 |
80.85 |
0 |
23.35 |
36.90 |
72.37 |
|
环己烷 |
3.95 |
8.45 |
19.15 |
100 |
76.65 |
63.10 |
27.63 |
下列说法错误的是
A.当温度超过280℃,苯的转化率迅速下降,可能是因为该反应为吸热的可逆反应
B.在110~240℃苯的转化率为100%。说明该镍催化剂活性较高,能够在较宽的温度范围内催化而且不发生副反应
C.增大压强与提高氢气、苯的物质的量比都有利于提高苯的转化率
D.由表中数据来看,随着反应温度的升高,苯的转化率先升高后降低
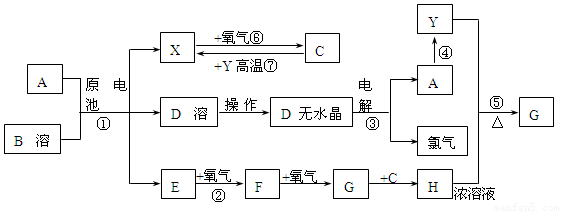
Ⅰ.氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答:
 (1)在一定体积的恒容密闭容器中,进行如下化学反应:
N2(g)+3H2(g) 2NH3(g)
(1)在一定体积的恒容密闭容器中,进行如下化学反应:
N2(g)+3H2(g) 2NH3(g)
其化学平衡常数K与温度t的关系如下表:
|
t/K |
298 |
398 |
498 |
… |
|
K/(mol·L-1)2 |
4.1×106 |
K1 |
K2 |
… |
完成下列问题:
①比较K1、K2的大小:K1 K2(填“>”、“=”或“<”)。
②判断该反应达到化学平衡状态的依据是 (填序号)。
A.2v(H2)(正)=3v(NH3)(逆) B.v(N2)(正)=3v(H2)(逆)C.容器内压强保持不变 D.混合气体的密度保持不变
(2)盐酸肼(N2H6Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。
①写出盐酸肼第一步水解反应的离子方程式 。
②盐酸肼水溶液中离子浓度的排列顺序正确的是 (填序号)。
A.c(Cl-)>c(N2H62+)>c(H+)>c(OH-)
B.c(Cl-)>c([N2H5·H2O+])> c(H+)>c(OH-)
C.c(N2H62+)+ c([N2H5·H2O+])+c(H+)= c(Cl-)+c(OH-)
D.c(N2H62+)> c(Cl-)>c(H+)>c(OH-)
Ⅱ.水体中重金属铅的污染问题备受关注。查资料得知Pb4+具有很强的氧化性。水中铅的存在形态主要有Pb2+、Pb(OH)+、Pb(OH)2(在水中溶解度小)、Pb(OH)3-、Pb(OH)42-,各形态的物质的量的分数α随溶液pH变化的关系如下图所示:
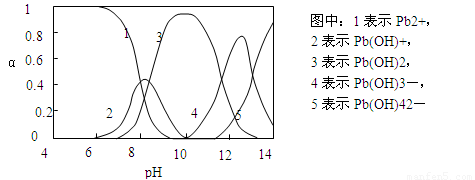
(1)Pb(NO3)2溶液中,c(Pb2+)/c(NO3-) 1/2(填“>”、“=”、“<”)。
(2)向Pb(NO3)2溶液滴加盐酸,溶液中c(Pb2+)/c(NO3-)没有变大,反而变小并有沉淀生成,则生成的沉淀可能为 。
(3)向Pb(NO3)2溶液中滴加NaOH溶液,溶液也变浑浊,在pH约为 时生成沉淀最多,继续滴加NaOH溶液,混合体系又逐渐变澄清。pH = 13时,混合体系中发生的主要反应的离子方程式为: 。


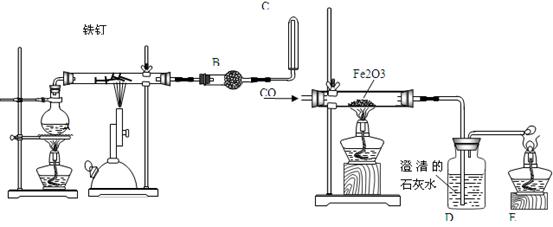
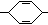
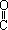 —H
—H —C≡C—
—C≡C—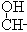
 A
A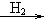 B
B C
C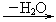 E:H—
E:H—