0 73902 73910 73916 73920 73926 73928 73932 73938 73940 73946 73952 73956 73958 73962 73968 73970 73976 73980 73982 73986 73988 73992 73994 73996 73997 73998 74000 74001 74002 74004 74006 74010 74012 74016 74018 74022 74028 74030 74036 74040 74042 74046 74052 74058 74060 74066 74070 74072 74078 74082 74088 74096 203614
 C(g)+2D(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述一定正确的是
C(g)+2D(g)达到平衡后,升高温度容器内气体的密度增大,则下列叙述一定正确的是

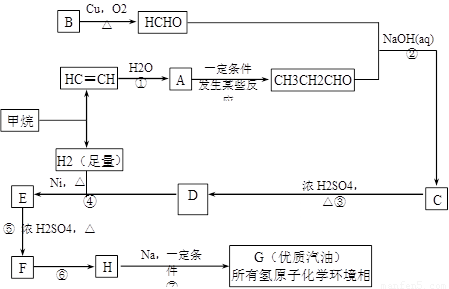
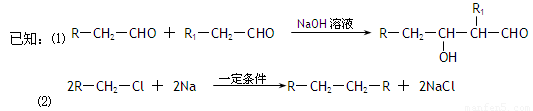
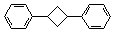 )的合成路线如下:
)的合成路线如下: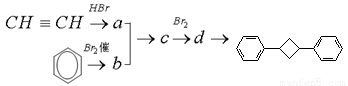

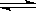 TiCl4(l)+O2 (g) ΔH=+151 kJ·mol-1所以不能直接由 TiO2 和 Cl2 反应(即氯化反应)来制取TiCl4。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
TiCl4(l)+O2 (g) ΔH=+151 kJ·mol-1所以不能直接由 TiO2 和 Cl2 反应(即氯化反应)来制取TiCl4。当往氯化反应体系中加入碳后,碳与上述反应发生耦合,使得反应在高温条件下能顺利进行。
 p
C(g);△H = a kJ/mol ( a<0);若在恒温、恒容下达到平衡时A的转化率为A1% ;在绝热、恒容条件下达到平衡时A的转化率为A2%,则A1和A2
的关系为
p
C(g);△H = a kJ/mol ( a<0);若在恒温、恒容下达到平衡时A的转化率为A1% ;在绝热、恒容条件下达到平衡时A的转化率为A2%,则A1和A2
的关系为