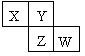下列说法正确的是
①热稳定性:HF>H2O>H2S ②离子半径:Na+>Mg2+>O2-
③碱性:Ca(OH)2>Mg(OH)2>NaOH
④相同物质的量浓度溶液的pH:NaOH>CH3COONa>NaCl
|
A.①③ |
B.②④ |
C.①④ |
D.②③ |
下列根据反应原理设计的应用,不正确的是
A.CO32- + H2O
 HCO3-+ OH- 热的纯碱溶液清洗油污
HCO3-+ OH- 热的纯碱溶液清洗油污
B.Al3+ + 3H2O  Al(OH)3 + H+ 明矾净水
Al(OH)3 + H+ 明矾净水
C.TiCl4+ (x+2)H2O(过量)  TiO2·x H2O↓ + 4HCl 用TiCl4制备TiO2
TiO2·x H2O↓ + 4HCl 用TiCl4制备TiO2
D.SnCl2 + H2O  Sn(OH)Cl↓ + HCl 配制氯化亚锡溶液时加入氢氧化钠
Sn(OH)Cl↓ + HCl 配制氯化亚锡溶液时加入氢氧化钠
下述实验不能达到预期目的的是
|
编号 |
实验内容 |
实验目的 |
|
A |
将AlCl3溶液蒸干灼烧 |
制备Al2O3[来源:Z_xx_k.Com] |
|
B |
向沸水中滴加几滴FeCl3饱和溶液,继续加热至红褐色 |
制备Fe(OH)3胶体 |
|
C |
向某溶液中加入稀H2SO4,将产生的气体通入澄清石灰水 |
检验溶液中是否含有 |
|
D |
相同温度下,测定浓度分别为0.1 |
比较 |
(12分)下表是短周期中部分元素的原子半径及主要化合价。
|
元素代号 |
W |
R |
X |
Y |
Z |
|
原子半径/nm |
0.037 |
0.157 |
0.066 |
0.070 |
0.077 |
|
主要化合价 |
+1 |
+1 |
-2 |
-3,+5 |
+2,+4 |
请回答:
(1)Z在元素周期表中的位置是 ,Z单质与Y的最高价氧化物对应水化物的浓溶液反应可生成一种红棕色气体,则反应的化学方程式为 。
(2)实验室制取YW3的化学方程式为 。
(3)R2X2与W2X反应的离子方程式为 ,若反应中转移的电子数为0.4×6.02×1023,则参加反应的R2X2的质量为 。
(4)X与Z组成一种有臭味的气体,与氧气按物质的量之比为1:2混合后恰好完全燃烧,生成稳定的氧化物,在同温同压下测得燃烧前后气体的总体积不变,则该反应的化学方程式是 。
(14分)已知:化合物B、C、E中含有两种相同的元素,A可用于玻璃、洗涤剂等的生产,B可用于制作光纤,G的组成元素与D相同。这些化合物之间存在下图所示的转化关系。
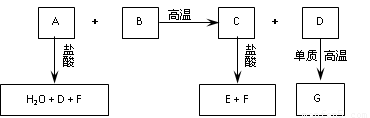
请回答:
(1)在化合物A、C、F中含有的相同元素 。
(2)化合物C的化学式为 ,其水溶液的pH 7(填“>”或“<”)。
(3) 700 ℃时,向容积为2 L的密闭容器中充入一定量的G(g)和H2O(g),发生反应:
G(g)+H2O(g)  D(g)+H2(g)。反应过程中测定的部分数据见下表(表中t1>t2):
D(g)+H2(g)。反应过程中测定的部分数据见下表(表中t1>t2):
|
反应时间/min |
n(G)/mol |
n(H2O)/ mol |
|
0 |
1.20 |
0.60 |
|
t1 |
0.80 |
|
|
t2 |
|
0.20 |
① 反应在t1min内的平均速率为v(H2)= mol/(L·min)
② 保持其他条件不变,起始时向容器中充入0.60 mol G和1.20 mol H2O,到达平衡时,
n(D)= mol。
③ 温度升至800℃,上述反应平衡常数为0.64,则正反应为 反应(填“放热”或“吸热”)。
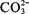
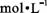 的Na2CO3和CH3COONa溶液的pH
的Na2CO3和CH3COONa溶液的pH 和
和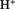 的能力强弱
的能力强弱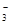 +5I
+5I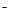 +3H2O=3I2+6OH
+3H2O=3I2+6OH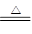 NH3↑+ 2H2O + CO32
NH3↑+ 2H2O + CO32