0 73663 73671 73677 73681 73687 73689 73693 73699 73701 73707 73713 73717 73719 73723 73729 73731 73737 73741 73743 73747 73749 73753 73755 73757 73758 73759 73761 73762 73763 73765 73767 73771 73773 73777 73779 73783 73789 73791 73797 73801 73803 73807 73813 73819 73821 73827 73831 73833 73839 73843 73849 73857 203614

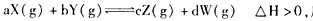 反应5min达到平衡时,X减小n mol·L-1,用Y表示的反应速率为0.6n mol·L-1·min-1。若将体系压强增大,W的百分含量不发生变化,则下列描述正确的是
(
)
反应5min达到平衡时,X减小n mol·L-1,用Y表示的反应速率为0.6n mol·L-1·min-1。若将体系压强增大,W的百分含量不发生变化,则下列描述正确的是
(
)
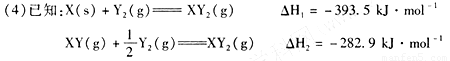
 该电池的负极反应式为 。
该电池的负极反应式为 。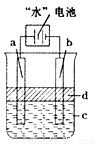
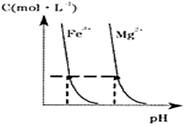
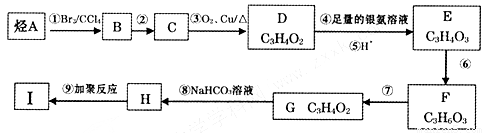
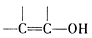 不能稳定存在。
不能稳定存在。