根据下列操作与产生的现象,所得结论正确的是
|
|
操作 |
现象 |
结论 |
|
A |
用洁净铂丝蘸取溶液进行焰色反应 |
火焰呈黄色 |
溶液中含Na+、无K+ |
|
B |
苯酚钠溶液中滴加稀盐酸 |
溶液变浑浊 |
苯酚的酸性比盐酸强 |
|
C |
用激光笔照射某有色玻璃 |
丁达尔现象 |
该有色玻璃是胶体 |
|
D |
AgCl饱和溶液中加入少量NaI溶液 |
产生黄色沉淀 |
Ksp(AgI)<Ksp(AgCl) |
(14分)工业上常回收冶炼锌废渣中的锌(含有ZnO、FeO、Fe2O3、CuO、Al2O3等杂质),并用来生产Zn(NO3)2·6H2O晶体,其工艺流程为:
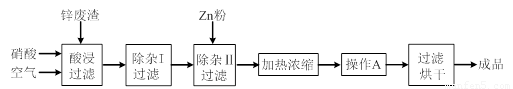
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
|
氢氧化物 |
Al(OH)3 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
Zn(OH)2 |
|
开始沉淀的pH |
3.3 |
1.5 |
6.5 |
4.2 |
5.4 |
|
沉淀完全的pH |
5.2 |
3.7 |
9.7 |
6.7 |
8.0 |
⑴在“酸浸”步骤中,为提高锌的浸出速率,除通入空气“搅拌”外,还可采取的措施是 ▲ 。
⑵上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有 ▲ 。
⑶在“除杂I”步骤中,需再加入适量H2O2溶液,H2O2与Fe2+反应的离子方程式为 ▲ 。为使Fe(OH)3 、Al(OH)3沉淀完全,而Zn(OH)2不沉淀,应控制溶液的pH范围为 ▲ 。检验Fe3+是否沉淀完全的实验操作是 ▲ 。
⑷加入Zn粉的作用是 ▲ 。“操作A”的名称是 ▲ 。
 D.0.15
mol NO2与水完全反应时转移的电子数为0.1NA
D.0.15
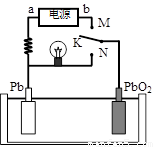
mol NO2与水完全反应时转移的电子数为0.1NA xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确的是
xC(g)+D(s),t1时达到平衡。在t2、t3时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化如图所示。下列说法正确的是