0 73474 73482 73488 73492 73498 73500 73504 73510 73512 73518 73524 73528 73530 73534 73540 73542 73548 73552 73554 73558 73560 73564 73566 73568 73569 73570 73572 73573 73574 73576 73578 73582 73584 73588 73590 73594 73600 73602 73608 73612 73614 73618 73624 73630 73632 73638 73642 73644 73650 73654 73660 73668 203614
 CH3OH(g) △H=-90.8 kJ/mol。
CH3OH(g) △H=-90.8 kJ/mol。 O2(g)
= H2O(g) △H=-241.8 kJ/mol
O2(g)
= H2O(g) △H=-241.8 kJ/mol CO(g)+2H2O(g)的反应热△H= ▲ 。
CO(g)+2H2O(g)的反应热△H= ▲ 。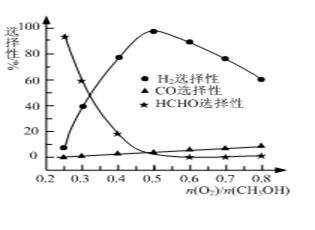

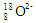
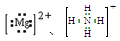
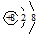
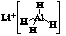 )、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125 ℃分解为LiH、H2和Al。下列说法不正确的是
)、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125 ℃分解为LiH、H2和Al。下列说法不正确的是