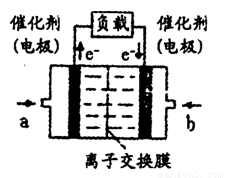
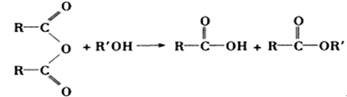
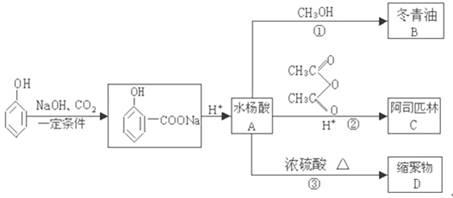
(16分)化学兴趣小组对某品牌牙膏中摩擦剂成分及其含量进行以下探究:
查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体生成。
I、摩擦剂中氢氧化铝的定性检验
取适量牙膏样品,加水搅拌、过滤。并进行如下实验
(1)、请完成表格中的填空:
|
实验步骤 |
实现现象 |
反应的离子方程式 |
|
往滤渣中加入过量NaOH溶液。 |
|
① |
|
过滤,往所得滤液中通入过量二氧化碳, |
② |
③ |
|
继续加入过量稀盐酸 |
④ |
|
II、牙膏样品中碳酸钙的定量测定
利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。
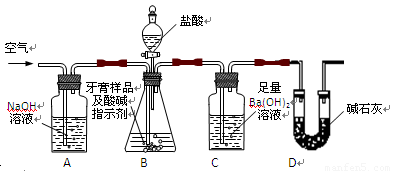
依据实验过程回答下列问题:
(2)、实验过程中先后两次鼓入空气,第二次鼓入空气的目的是:
。
(3)、C中反应生成BaCO3的化学方程式是 。
(4)、下列各项措施中,不能提高测定准确度的是 (填标号)。
A.在加入盐酸之前,应排净装置内的CO2气体
B.滴加盐酸不宜过快
C.在A—B之间增添盛有浓硫酸的洗气装置
D.在B—C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(5)、实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g.则样品中碳酸钙的质量分数为 。
(6)、某同学提出将C中的Ba(OH)2换成浓H2SO4 ,通过测定D装置反应前后的质量差也可以测定CaCO3的含量,假设反应前D装置的质量为m1,实验结束后D装置的质量为m2,则样品中CaCO3的质量为 。实验证明按此测定的结果偏高,原因是 。
(选修—化学与技术)(15分)
(1)工业上以粗铜为原料采取如图1所示流程制备硝酸铜晶体:
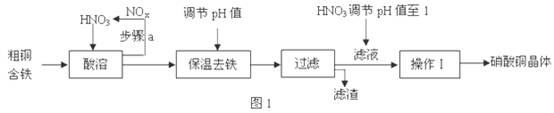
①在步骤a中,还需要通入氧气和水,其目的是 。
②在保温去铁的过程中,为使Fe3+沉淀完全,根据下表数据,溶液的pH值应保持在 范围。调节pH值时,可以向溶液中加入的试剂是( )
(a) NaOH溶液 (b) 氨水 (c) Cu(OH)2 (d) CuO
|
|
氢氧化物开始沉淀时的pH |
氢氧化物沉淀完全时的pH |
|
Fe3+ Cu2+ |
1.9 4.7 |
3.2 6.7 |
③在操作Ⅰ之前,对滤液用HNO3调节pH值至1,其目的是(结合离子方程式说明) 。
④从滤液中制取硝酸铜晶体的操作Ⅰ的具体步骤是 。
(2)图2是某小组学生查阅资料后所绘出的硝酸铜晶体[Cu(NO3)2 nH2O]的溶解度曲线(温度在300C左右对应不同的晶体),下列说法正确的是( )
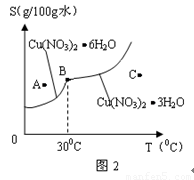
(a) A点时的溶液为不饱和溶液
(b) B点时两种晶体可以共存
(c)按上述流程最终得到的晶体一定是Cu(NO3)2 3H2O
(d) 若将C点时的溶液降温至300C以下,可以析出Cu(NO3)2 6H2O晶体

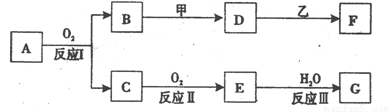
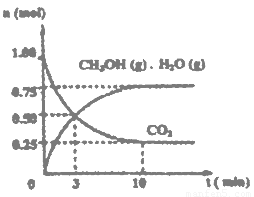

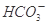 +H+的电离平衡常数 K=____________。(已知:10-5.6=2.5×10-6)。
+H+的电离平衡常数 K=____________。(已知:10-5.6=2.5×10-6)。