(10分)铁单质及其化合物在生活、生产中应用广泛。请回答下列问题:
(1)钢铁在空气中发生吸氧腐蚀时,正极的电极反应式为______________________。
(2)由于氧化性Fe3+>Cu2+,氯化铁溶液常用作印刷电路铜板腐蚀剂,反应的离子方程式是________。
(3)硫酸铁可作絮凝剂,常用于净水,其原理是______________________(用离子方程式表示)。在使用时发现硫酸铁不能使酸性废水中的悬浮物沉降而除去,其原因是__________。
(4)磁铁矿是工业上冶炼铁的原料之一,其原理是Fe3O4+4CO===3Fe+4CO2,若有1.5 mol Fe3O4参加反应,转移电子的物质的量是__________________。
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是________(填字母)。
|
选项 |
陈述Ⅰ |
陈述Ⅱ |
判断 |
|
A |
铁是地壳中含量最高的 金属元素 |
铁是人类最早使用的金属材料 |
Ⅰ对;Ⅱ对;有 |
|
B |
常温下铁与稀硫酸反应 生成氢气 |
高温下氢气能还原氧化 铁得到铁 |
Ⅰ对;Ⅱ对;无 |
|
C |
铁属于过渡元素 |
铁和铁的某些化合物可用作催化剂 |
Ⅰ错;Ⅱ对;无 |
|
D |
在空气中铁的表面能形 成致密的氧化膜 |
铁不能与氧气反应 |
Ⅰ对;Ⅱ对;有 |
(10分)X、Y、Z、M、R、Q是短周期主族元素,部分信息如下表所示:
|
|
X |
Y |
Z |
M |
R |
Q |
|
原子半径/nm |
|
|
0.186 |
0.074 |
0.099 |
0.143 |
|
主要化合价 |
|
-4,+4 |
|
-2 |
-1,+7 |
+3 |
|
其它 |
阳离子核外无电子 |
无机非金属材料的主角 |
焰色反应呈黄色 |
|
|
|
(1)R在元素周期表中的位置是__________________。
(2)Y与R相比,非金属性较强的是 (用元素符号表示),下列事实能证明这一结论的是 (选填字母序号)。
a.常温下Y的单质呈固态,R的单质呈气态
b.稳定性.XR>YX4
c.Y与R形成的化合物中Y呈正价
(3)根据表中数据推测,Y的原子半径的最小范围是__________________.
(4)甲、乙是上述部分元素的最高价氧化物对应的水化物,且甲+乙→丙+水。若丙的水溶液呈碱性,则丙的化学式是____________或____________.
(8分)已知:

(1)该反应的生成物中含有的官能团的名称是__________,该物质在一定条件下能发生_______(填序号)。
①氧化反应 ②还原反应 ③酯化反应
(2)已知HCHO分子中所有原子都在同一平面内,若要使R1CHO分子中所有原子可能都在同一平面内,R1可以是________(填序号)。
 ①—CH3 ② ③—CH═CH2
①—CH3 ② ③—CH═CH2
(3)某氯代烃A的分子式为C6H11Cl,它可以发生如下转化:
 |
结构分析表明E分子中含有两个甲基且没有支链。
①写出A B的化学方程式:
B的化学方程式:
②E的结构简式为:
③写出D的同时符合下列条件的同分异构体的结构简式: a.属于二元醇; b.主链上有4个碳原子;


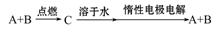


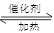 7N2+12
H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
L。
7N2+12
H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
L。 2SO3(g) ΔH=-196.6
kJ·mol-1
2SO3(g) ΔH=-196.6
kJ·mol-1