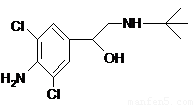
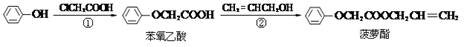某学习小组根据化学知识和下表的数据,设计了表中的实验,以验证酸性:盐酸>碳酸>苯酚>碳酸氢根离子,其中不合理的是 ( )
|
物质 |
电离常数 |
和溶解度(25℃) |
|
C6H5OH |
K =1.28×10-10 |
S = 9.3g/100g水 |
|
H2CO3 |
K1 =4.3×10-7 |
|
|
K2 =5.6×10-11 |
|
|
|
组别 |
操作 |
判断依据 |
|
A |
盐酸和碳酸 |
往碳酸钙固体中滴加盐酸 |
观察有无气体产生 |
|
B |
碳酸与苯酚 |
往苯酚钠饱和溶液中,通入足量CO2 |
观察溶液是否变浑浊 |
|
C |
碳酸与苯酚 |
配制同物质的量浓度的碳酸钠溶液和苯酚钠溶液 |
比较溶液的pH |
|
D |
HCO3-与苯酚 |
在苯酚悬浊液中,加入过量的 Na2CO3溶液 |
观察悬浊液是否变澄清 |
.25℃时,弱酸的电离平衡常数如右表,下列说法正确的是( )
|
弱酸 |
CH3COOH |
HCN |
H2CO3 |
|
K |
1.8×10-5 |
4.9×10-10 |
K1=4.3×10-7 K2=5.6×10-11 |
A.等物质的量浓度溶液pH关系: pH(NaCN)> pH(Na2CO3)> pH(CH3COONa)
B.amol/L HCN与bmol/L NaOH溶液等体积混合后所得溶液中c(Na+)>c(CN-),则a一定小于b
C.往冰醋酸中逐滴加水,溶液导电能力先增大,后减小
D.NaHCO3和Na2CO3的混合液中:c(Na+)+c(H+)=c(OH-)+c(HCO-3)+c(CO32-)
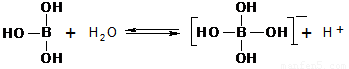

 A.试剂X为稀硫酸,沉淀中含有硅的化合物
A.试剂X为稀硫酸,沉淀中含有硅的化合物