0 73322 73330 73336 73340 73346 73348 73352 73358 73360 73366 73372 73376 73378 73382 73388 73390 73396 73400 73402 73406 73408 73412 73414 73416 73417 73418 73420 73421 73422 73424 73426 73430 73432 73436 73438 73442 73448 73450 73456 73460 73462 73466 73472 73478 73480 73486 73490 73492 73498 73502 73508 73516 203614
 2NO(g) K1=1×10-30 ㈠
2NO(g) K1=1×10-30 ㈠ ①常温下,反应2H2O(g)
2H2(g) +O2(g) 平衡常数K= ;
①常温下,反应2H2O(g)
2H2(g) +O2(g) 平衡常数K= ;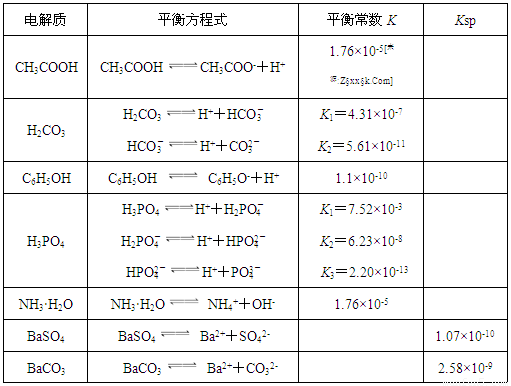
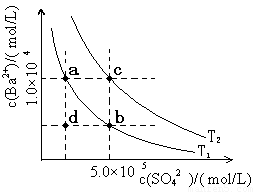
 BaCO3(s)+ SO42- (aq) ]
BaCO3(s)+ SO42- (aq) ]