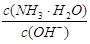0 72814 72822 72828 72832 72838 72840 72844 72850 72852 72858 72864 72868 72870 72874 72880 72882 72888 72892 72894 72898 72900 72904 72906 72908 72909 72910 72912 72913 72914 72916 72918 72922 72924 72928 72930 72934 72940 72942 72948 72952 72954 72958 72964 72970 72972 72978 72982 72984 72990 72994 73000 73008 203614
 的浓度为C3 , 则它们之间的关系是
的浓度为C3 , 则它们之间的关系是 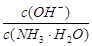 B.
B.