(6分)自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。
(1)在不同温度下,反应N2(g)+O2(g) 2NO(g) DH=a kJ·mol-1的平衡常数K如下表:
2NO(g) DH=a kJ·mol-1的平衡常数K如下表:
|
温度/℃ |
1538 |
1760 |
2404 |
|
平衡常数K |
0.86×10-4 |
2.6×10-4 |
64×10-4 |
该反应的△H 0(填“>”、“=”或“<”)。
(2)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应:
N2(g)+O2(g)
 2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
2NO(g)达到平衡时N2的浓度为 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
(3)科学家一直致力于研究常温常压下“人工固氮”的新方法。曾有实验报道:在常温、常压光照条件下,N2在催化剂(掺有少量Fe2O3的TiO2)表面与水发生反应,生成的主要产物为NH3。相应的热化学方程式如下:
2N2(g)+6H2O(1)=4NH3 (g)+3O2(g) DH=+1530kJ·mol-1
则氨催化氧化反应4NH3(g)+5O2(g)=4NO(g)+6H2O(1)的反应热DH= 。 (用含a的代数式表示)
Ⅰ.(4分)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
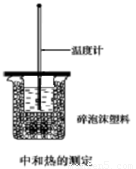
(1)从实验装置上看,图中尚缺少的一种玻璃用品 是 。
(2)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会 ;(填“偏大”、“偏小”、“无影响”)。
(3)如果反应前后的温度差是(t2-t1),盐酸、氢氧化钠溶液的密度均为1g/cm3,比热容为 4.18J/(g•℃),写出该实验中和热的计算式:△H=
Ⅱ.(12分)影响化学反应速率的因素很多,某校化学小组用实验的方法进行探究。
实验一:他们只利用Cu、Fe、Mg和不同浓度的硫酸(0.5 mol/L、2 mol/L、18.4 mol/L)。设计实验方案来研究影响反应速率的因素。
甲同学研究的实验报告如下表:
|
实验步骤 |
现象 |
结论 |
|
①分别取等体积的2 mol/L的硫酸于试管中 |
反应速率Mg>Fe,Cu不反应 |
金属的性质越活泼,反应速率越快 |
|
②___________________ |
(1)甲同学表中实验步骤②为____________________________________________。
(2)甲同学的实验目的是______________________________________;要得出正确的实验结论,还需控制的实验条件是________。
乙同学为了更精确的研究浓度对反应速率的影响,利用下图所示装置进行定量实验。
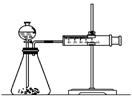
(3)乙同学在实验中应该测定的数据是______________。
(4)乙同学完成该实验应选用的实验药品是___________。
该实验中不选用某浓度的硫酸,理由是____________。
下列物质的分类组合全部正确的是
|
编组 |
强电解质 |
弱电解质 |
非电解质 |
|
A |
NaCl |
HF |
Cl2 |
|
B |
H2SO4 |
BaSO4 |
CS2 |
|
C |
NH3·H2O |
HClO |
Cu |
|
D |
Ba(OH)2 |
H2S |
C2H5OH |
 2B(g)和2C(g)
2B(g)和2C(g)  pC达到平衡,若:
pC达到平衡,若: 2SO3(g),反应过程的能量变化如下图所示。已知1mol SO2(g)氧化为1 mol SO3(g)的△H=–99
kJ/mol。请回答下列问题:
2SO3(g),反应过程的能量变化如下图所示。已知1mol SO2(g)氧化为1 mol SO3(g)的△H=–99
kJ/mol。请回答下列问题: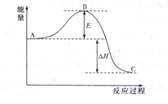
 B(g)+D(s)在四种不同条件下进行,反应器均为相同恒容密闭容器,B、D起始为0。反应物A的浓度(mol·L−1)随反应时间(min)的变化情况如下表:
B(g)+D(s)在四种不同条件下进行,反应器均为相同恒容密闭容器,B、D起始为0。反应物A的浓度(mol·L−1)随反应时间(min)的变化情况如下表: