(9分)下表是元素周期表的一部分,针对表中的①~⑩中元素,填写下列空格:
|
|
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
2 |
|
|
|
① |
② |
③ |
④ |
|
|
3 |
|
⑤ |
⑥ |
⑦ |
|
⑧ |
⑨ |
⑩ |
(1)在这10种元素中,化学性质最不活泼的元素是 (填元素符号),金属性最强的元素是 (填元素名称),最活泼的非金属单质是 (化学式),元素⑨对应的离子结构示意图为 _。
(2)给出的第二周期的几种元素中,原子半径最大的是 (填元素符号)。
(3)元素③与⑧的气态氢化物中较稳定的物质是 (填该物质的电子式)。
(4)元素⑤与⑥的最高价氧化物的水化物中,碱性较强的物质是 (填化学式)。
(5)元素③与⑦能以 键(填化学键类型)结合成 晶体(填晶体类型)。
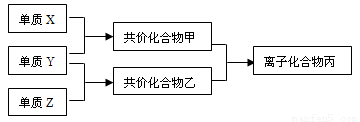
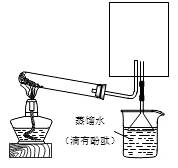

 2H2↑+O2↑。制得的氢气可用于燃料电池。
2H2↑+O2↑。制得的氢气可用于燃料电池。
