(14分)某化学实验小组想要了解市场上所售食用白醋(主要是醋酸的水溶液)的准确浓度,现从市场上买来一瓶某品牌食用白醋,在实验室中用标准NaOH溶液对其进行滴定。下表是4种常见指示剂的变色范围:
|
指示剂 |
石蕊 |
甲基橙 |
甲基红 |
酚酞 |
|
变色范围(pH) |
5.0~8.0 |
3.1~4.4 |
4.4~6.2 |
8.2~10.0 |
(1)向锥形瓶中移取一定体积的白醋所用的仪器是 ,该实验最佳应选用
作指示剂,达到滴定终点的实验现象是: 。
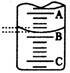
(2)如图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的刻度为25,滴定管中液面读数应为 mL,此时滴定管中液体的体积 。
(3)为了减小实验误差,该同学一共进行了三次实验,假设每次所取白醋体积均为VmL,NaOH标准液浓度为c mo1/L,三次实验结果记录如下:
|
实验次数 |
第一次 |
第二次 |
第三次 |
|
消耗NaOH溶液体积/mL |
26.02 |
25.35 |
25.30 |
从上表可以看出,第一次实验中记录消耗NaOH溶液的体积明显多于后两次,其原因可能是
A.实验结束时俯视滴定管中液面,读取滴定终点时NaOH溶液的体积
B.滴加NaOH溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定
C.盛装标准液的滴定管装液前用蒸馏水润洗过,未用标准液润洗
D.第一次滴定用的锥形瓶用待装液润洗过,后两次未润洗,
(4)根据所给数据,写出计算该白醋中醋酸的物质的量浓度的表达式(不必化简):
C= 。
 Ur﹣(尿酸根离子)+H3O+ Ur﹣(溶液)+Na+(溶液)
Ur﹣(尿酸根离子)+H3O+ Ur﹣(溶液)+Na+(溶液)
 2NH3(g)
ΔH < 0 正、逆反应的平衡常数K随温度的变化
2NH3(g)
ΔH < 0 正、逆反应的平衡常数K随温度的变化  I2+2 Fe2+设计成如图所示的原电池。下列判断不正确的是
I2+2 Fe2+设计成如图所示的原电池。下列判断不正确的是
 B 电流计读数为零时,反应达到化学平衡状态
B 电流计读数为零时,反应达到化学平衡状态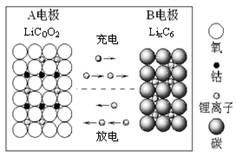
 Li1-xCoO2+LixC6
Li1-xCoO2+LixC6 ,利用此概念可以讨论许多化学问题:
,利用此概念可以讨论许多化学问题: 4NO(g)+6H2O(g);假如温度保持不变并充入He,则平衡
(填“正向移动”、“逆向移动”、“不移动”),
4NO(g)+6H2O(g);假如温度保持不变并充入He,则平衡
(填“正向移动”、“逆向移动”、“不移动”), (混合气)将
(填写“变大”、“变小”或“不变”);
(混合气)将
(填写“变大”、“变小”或“不变”); C(g)+D(g)已达平衡的是
C(g)+D(g)已达平衡的是 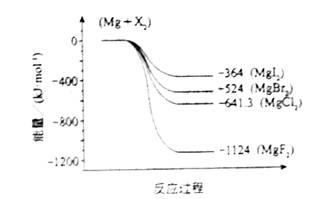
 HCO3- + H+
Ka1(H2CO3) = 4.45×10-7
HCO3- + H+
Ka1(H2CO3) = 4.45×10-7 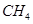 (g)+
(g)+ 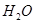 (g)=
(g)=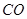 (g)+
(g)+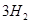 (g)
(g) 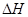 =
+
=
+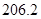

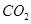 (g)=
(g)=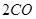 (g)+
(g)+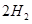 (g)
(g)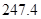
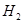 (g)的热化学方程式为
。
(g)的热化学方程式为
。 O的热分解也可得到H
O的热分解也可得到H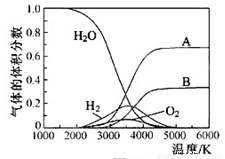
 CH3OH(气),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,求:(1)H2的反应速率;(2)CO的转化率;(3)求相同条件下CH3OH(气)
CH3OH(气),6秒时体系达到平衡,此时容器内压强为开始时的0.6倍,求:(1)H2的反应速率;(2)CO的转化率;(3)求相同条件下CH3OH(气)