(1)工业上一般采用下列两种反应合成甲醇:
反应I: CO(g) + 2H2(g)  CH3OH(g); ΔH1
CH3OH(g); ΔH1
反应II: CO2(g) + 3H2(g)  CH3OH(g)
+H2O(g);ΔH2
CH3OH(g)
+H2O(g);ΔH2
① 上述反应符合“原子经济”原则的是 (填“I”或“Ⅱ”)。
② 下表所列数据是反应I在不同温度下的化学平衡常数(K)。
|
温度 |
250℃ |
300℃ |
350℃ |
|
K |
2.041 |
0.270 |
0.012 |
由表中数据判断ΔH1 0 (填“>”、“=”或“<”)。
③ 某温度下,将2 mol CO和6 mol H2充入2L的密闭容器中,充分反应,达到平衡后,测得c(CO)= 0.2 mol/L,则CO的转化率为 ,此时的温度为 (从上表中选择)。
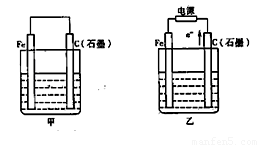
(2)某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。
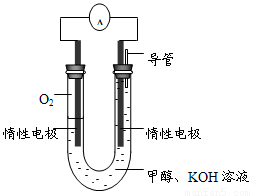
①该电池正极通入的物质为 。
② 工作一段时间后,测得溶液的pH减小,该电池总反应的化学方程式为
现有部分前四周期元素的性质或原子结构如下表:
|
元素编号 |
元素性质或原子结构 |
|
A |
第三周期中的半导体材科 |
|
B |
L层s电子数比p电子数少l |
|
C |
地壳中含量最高的元素 |
|
D |
第三周期主族元素中其第一电离能最大 |
|
E |
第四周期中未成对电子数最多 |
( 1)写出元素E基态原子的电子排布式: ,基态C原子的价电子轨道表示式是 。
(2)B单质分子中,含有 个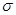 键和 个
键和 个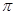 键。元素B的气态氢化的空间构型
键。元素B的气态氢化的空间构型
为 ,其中B原子的杂化方式是
(3)A、B、C第一电离由大到小的顺序为(用元素符号表示): ;
(4)将B的氢化物的水溶液逐滴加入到CuSO4溶液中直到过量,观察到的现象是 ,相关的离子方程式是 。
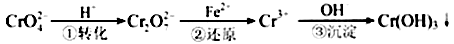
 Cr2O72—(橙色)+H2O
Cr2O72—(橙色)+H2O