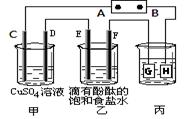
一定温度下,容积为2 L的甲、乙两固定容积的密闭容器中,发生反应:
2SO2(g)+O2(g)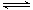 2SO3(g)。达平衡时测得有关数据如下表。
2SO3(g)。达平衡时测得有关数据如下表。
|
容 器 |
甲 |
乙 |
|
反应物投入量 |
2 mol SO2、1 mol O2 |
4 mol SO3 |
|
n(SO3)/mol |
1.6 |
a |
|
反应物的转化率 |
α1 |
α2 |
下列说法正确的是
A.α1+α2>1
B.1.6<a<3.2
C.若甲中反应2 min时达到平衡,则2 min 内平均速率ν(O2)= 0.1 mol·L-1·min-1
D.甲平衡后再加入0.2 mol SO2、0.2 mol O2和0.4 mol SO3,平衡正向移动
相同温度下,体积均为0.25 L的两个恒容密闭容器中发生可逆反应:N2(g)+3H2(g) 
 2NH3(g) ΔH=-92.6 kJ/mol。实验测得起始、平衡时的有关数据如下表所示:
2NH3(g) ΔH=-92.6 kJ/mol。实验测得起始、平衡时的有关数据如下表所示:
|
容器编号 |
起始时各物质的物质的量/mol |
达平衡时体系能量的变化 |
||
|
N2 |
H2 |
NH3 |
||
|
① |
1 |
3 |
0 |
放出热量:23.15 kJ |
|
② |
0.9 |
2.7 |
0.2 |
放出热量:Q |
下列叙述错误的是 ( )
A.容器①、②中反应的平衡常数相等
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器②中达平衡时放出的热量Q=23.15 kJ
D.若容器①的体积为0.5 L,则平衡时放出的热量小于23.15 kJ
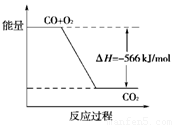
 nY(g); ΔH=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
nY(g); ΔH=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
 Z(g);△H <0 下图是表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5
时刻外界条件有所改变,但都没有改变各物质的用量。则下列说法中不正确的是
Z(g);△H <0 下图是表示该反应的速率(v)随时间(t)变化的关系图,t2、t3、t5
时刻外界条件有所改变,但都没有改变各物质的用量。则下列说法中不正确的是