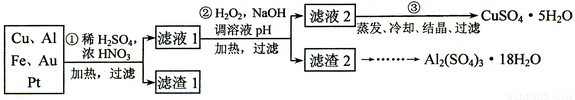
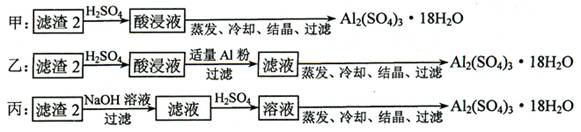
完成下列实验所选择的装置或仪器(夹持装置已略去)正确的是
|
|
A |
B |
C |
D |
|
实 验 |
用CCl4提取 溴水中的Br2 |
除去乙醇 中的苯酚 |
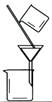
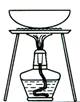
从KI和I2的固体 混合物中回收I2 |
配制100 mL 0.1000 mol·L-1 K2Cr2O7溶液 |
|
装 置 或 仪 器 |
|
|
|
|
(14分)金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:
WO3 (s) + 3H2 (g)  W (s) + 3H2O (g)
W (s) + 3H2O (g)
请回答下列问题:
⑴ 上述反应的化学平衡常数表达式为___________________________。
⑵ 某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为_____________________;随温度的升高,H2与水蒸气的体积比减小,则该反应为___________反应(填“吸热”或“放热”)。
⑶上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
|
温度 |
25℃ ~ 550℃ ~ 600℃ ~ 700℃ |
|
主要成份 |
WO3 W2O5 WO2 W |
第一阶段反应的化学方程式为___________________________;580℃时,固体物质的主要成分为________;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为____________________________________。
⑷ 已知:温度过高时,WO2 (s)转变为WO2 (g);
WO2 (s) + 2H2 (g)  W (s) + 2H2O (g)
ΔH = +66.0 kJ·mol-1
W (s) + 2H2O (g)
ΔH = +66.0 kJ·mol-1
WO2 (g) + 2H2(g)  W (s) + 2H2O (g)
ΔH = -137.9 kJ·mol-1
W (s) + 2H2O (g)
ΔH = -137.9 kJ·mol-1
则WO2 (s)  WO2 (g) 的ΔH =
______________________。
WO2 (g) 的ΔH =
______________________。
⑸ 钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:W (s) +2I2 (g) 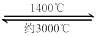 WI4 (g)。下列说法正确的有________________。
WI4 (g)。下列说法正确的有________________。
a.灯管内的I2可循环使用
b.WI4在灯丝上分解,产生的W又沉积在灯丝上
c.WI4在灯管壁上分解,使灯管的寿命延长
 d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
d.温度升高时,WI4的分解速率加快,W和I2的化合速率减慢
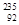 U和
U和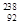 U是中子数不同质子数相同的同种核素
U是中子数不同质子数相同的同种核素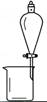

 )
) 2SO3 (g);ΔH = -197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2
;(丙) 2 mol SO3 。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3 (g);ΔH = -197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2
;(丙) 2 mol SO3 。恒温、恒容下反应达平衡时,下列关系一定正确的是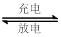 Fe
+ 2ZG
Fe
+ 2ZG