常温下,把2.7g铝投入到一定量氢氧化钠溶液中,充分反应后,下列表示正确的是(NA为阿佛加德罗常数)
|
|
电子转移 |
反应的Al |
溶液中的AlO2- |
生成的H2 |
|
A |
0.2NA |
|
|
0.1NA |
|
B |
0.3NA |
|
0.3NA |
|
|
C |
|
2.7g |
|
3.36L |
|
D |
0.1NA |
2.7g |
|
|
现有一瓶甲、乙的混合物,已知甲、乙属同系物,甲、乙某些性质如下:
|
物质 |
分子式 |
熔点(℃) |
沸点(℃) |
密度(g/cm3) |
水溶性 |
|
甲 |
C3H6O2 |
-98 |
57.5 |
0.93 |
可溶 |
|
乙 |
C4H8O2 |
-84 |
77 |
0.90 |
可溶 |
根据物理性质,将混合物中甲、乙分离的最佳方法是
A.蒸馏 B.萃取 C.加热升华 D.分液
已知某化学反应的平衡常数表达式为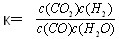 ,在不同的温度下该反应的平衡常数值分别为:
,在不同的温度下该反应的平衡常数值分别为:
|
t℃ |
700 |
800 |
830 |
1000 |
1200 |
|
K |
1.67 |
1.11 |
1.00 |
0.60 |
0.38 |
有关叙述错误的是
A.该反应的化学方程式是:CO(g)+H2O(g) 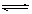 CO2(g)+H2(g)
CO2(g)+H2(g)
B.该反应的正反应是放热反应
C.如果在一定体积的密闭容器中加入CO和H2O各1 mol,再把温度升高到830 ℃,此时测得CO2为0.4 mol时,这时可逆反应处于平衡状态
D.若平衡浓度关系符合 =
=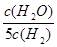 ,可判断此时温度是1000 ℃
,可判断此时温度是1000 ℃
将固体MnC2O4·2H2O放在坩埚里加热,固体质量随温度变化的数据如下表:
|
温度(℃) |
25 |
50 |
75 |
100 |
214 |
280 |
|
固体质量(g) |
17.9 |
17.9 |
16.0 |
14.3 |
14.3 |
7.10[ |
下列说法错误的是
A.25~50 ℃,MnC2O4·2H2O未发生变化
B.75 ℃时,MnC2O4·2H2O部分失去结晶水
C.100℃时,坩埚内固体均为MnC2O4
D.280℃时,坩埚内固体为混合物
 CaCO3↓
+ CO2↑ + H2O
CaCO3↓
+ CO2↑ + H2O