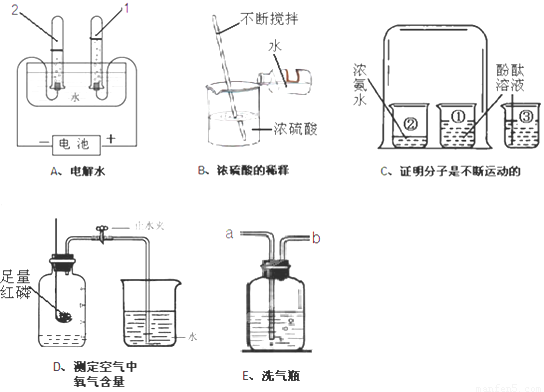
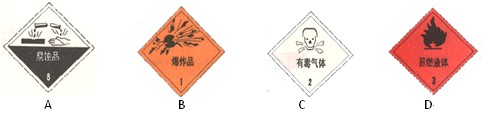
(10分)某化学兴趣小组为了测定镁铜合金中镁的质量分数,取出3g合金样品,将60g稀硫酸分6次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
|
稀硫酸用量 |
剩余固体质量 |
|
第一次加入10g |
mg |
|
第二次加入10g |
2.0g |
|
第三次加入10g |
1.5g |
|
第四次加入10g |
1.0g |
|
第五次加入10g |
0.6g |
|
第六次加入10g |
0.6g |
(1)从以上数据可知,最后剩余的0.6g固体的成分是 ;这六次实验中,第 次加入稀硫酸时样品中的镁已经完全反应;表格中,m= 。
(2)计算合金样品中镁的质量分数。
(3)计算所用稀硫酸中H2SO4的质量分数。
社会实践活动中,课外兴趣小组对某钢铁厂的铁矿石样品和钢样进行实验、分析、计算,了解了该钢铁厂生产原料、产品的相关信息。下面请你根据他们的实验帮助计算回答:
取该厂的某钢样粉末28.36 g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到3 g白色沉淀。
(1)计算此钢样粉末中铁和碳的质量之比。
(2)再取三份不同质量的钢样粉末分别加到50 g质量分数相同的硫酸中,充分反应后,测得的实验数据如下表所示:(标准状况下,2 g H2的体积为22.4 L)
|
实验序号 |
Ⅰ |
Ⅱ |
Ⅲ |
|
加入钢样粉末的质量 / g |
2.836 |
5.672 |
8.508 |
|
生成气体的体积(标准状况)/ L |
1.12 |
2.24 |
2.80 |
请根据表中数据计算硫酸中H2SO4的质量分数。
(3)若在实验Ⅱ中继续加入m g钢样粉末,计算反应结束后剩余的固体质量为多少? (用含m的代数式表示)