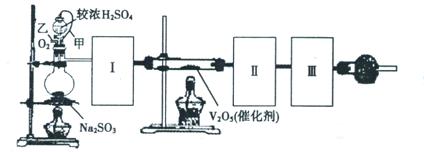
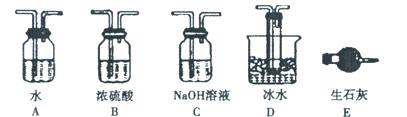
某无色溶液中可能含有①Na+、②Ba2+、③Cl-、④Br-、⑤SO32-、⑥SO42-中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
|
步骤 |
操作 |
现象 |
|
(1) |
用pH试纸检验 |
溶液pH大于7 |
|
(2) |
向溶液中滴加氯水,再加入CCl4振荡,静置 |
CCl4层呈橙色 |
|
(3) |
向(2)所得的水溶液中加入 Ba(NO3)2和稀HNO3 |
有白色沉淀产生 |
|
(4) |
过滤,向滤液中加入AgNO3溶液和稀HNO3 |
有白色沉淀产生 |
下列结论正确的是
A.肯定含有的离子是①④⑤ B.肯定没有的离子是②⑤
C.不能确定的离子是① D.不能确定的离子是③⑤
下图所示是验证氯气性质的微型实验,a、b、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl→2KCl+5Cl2↑+2MnCl2+8H2O

对实验现象的“解释或结论”正确的是
|
选项 |
实验现象 |
解释或结论 |
|
A |
a处变蓝,b处变红棕色 |
氧化性:Cl2>Br2>I2 |
|
B |
c处先变红,后褪色 |
氯气与水生成了酸性物质 |
|
C |
d处立即褪色 |
氯气与水生成了漂白性物质 |
|
D |
e处变红色 |
还原性:Fe2+>Cl- |
(12分)A、B、C、D、E、F、G七种物质间存在如图所示的转化关系,其中A、B、D、G含有同种元素。已知:(Ⅰ)A为金属单质; B为红褐色固体;E为密度最小的气体;G为浅绿色溶液。

(Ⅱ)D为黄色溶液,能与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀。
(Ⅲ)D能将某种氧化物氧化为F,F是含有三种元素的化合物。
请回答下列问题:
(1)上述反应中属于置换反应的是 (填序号)。
(2)G生成B有多种途径。若在G的溶液中加入与G等物质的量的Na2O2,恰好使G转化为F,写出该反应的离子方程式:
反应③(即D将某种氧化物氧化为F)的离子方程式
(3)实验室制取C的化学方程式为
对气体C进行如下实验。已知整个反应过程中,每消耗0.1mol KI,转移的电子数约为3.612×1023 个。请按照要求填空:
|
实验步骤 |
实验现象 |
用化学用语解释 |
|
将少量气体通入淀粉KI溶液 |
溶液最初变成 色 |
(用离子方程式表示) |
|
继续通入气体 |
溶液逐渐变成无色 |
(用化学方程式表示) |