下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断以下叙述正确的是
|
元素代号 |
A |
B |
C |
D |
E |
|
原子半径/nm |
0.160 |
0.143 |
0.102 |
0.071 |
0.099 |
|
主要化合价 |
+2 |
+3 |
+6、-2 |
-1 |
-1 |
A.A、B的单质与稀盐酸反应速率B>A
B.D、E形成的简单离子的还原性E->D-
C.气态氢化物的稳定性HD<H2C
D.最高价氧化物对应的水化物的酸性 H2CO4>HEO4
根据表中信息,判断下列叙述中正确的是
|
序号 |
氧化剂 |
还原剂 |
其他反应物 |
氧化产物 |
还原产物 |
|
① |
Cl2 |
FeBr2 |
/ |
|
Cl- |
|
② |
KClO3 |
浓盐酸 |
/ |
Cl2 |
|
|
③ |
KMnO4 |
H2O2 |
H2SO4 |
O2 |
Mn2+ |
A.表中①组的反应可能有一种或两种元素被氧化
B.氧化性强弱的比较: KClO3>Fe3+>Cl2>Br2
C.表中②组反应的还原产物是KCl,电子转移数目是6e-
D.表中③组反应的离子方程式为:2MnO4-+ 3H2O2 + 6H+=2Mn2+ + 4O2↑+ 6H2O
下列实验“操作和现象”与“结论”都正确的是
|
|
操作和现象 |
结论 |
|
A |
切开金属钠,钠表面的银白色会逐渐褪去 |
Na在空气中会生成Na2O2 |
|
B |
铝箔插入浓硝酸中,无明显现象 |
铝与浓硝酸不反应 |
|
C |
SO2通入酸性KMnO4溶液,溶液褪色 |
SO2具有漂白性 |
|
D |
将充满NO2的试管倒立在水中,试管内液面约上升至试管容积的2/3处;缓慢通入O2,轻轻晃动试管,至液体基本上充满试管 |
从原料的充分利用和减少污染物的排放等方面考虑,该实验对工业生产硝酸有重要启示 |
已知:KClO3+6HCl(浓)===KCl+3Cl2↑+3H2O。如下图所示,将少量试剂分别放入培养皿中的相应位置,实验时将浓盐酸滴在KClO3晶体上,并用表面皿盖好。下表中由实验现象得出的结论完全正确的是

|
选项 |
实验现象 |
结论 |
|
A |
滴有KSCN的FeCl2溶液变红 |
Cl2具有还原性 |
|
B |
滴有酚酞的NaOH溶液褪色 |
Cl2具有酸性 |
|
C |
石蕊溶液先变红后褪色 |
Cl2具有漂白性 |
|
D |
KI-淀粉溶液变蓝 |
Cl2具有氧化性 |

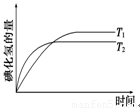
 2HI(g),在温度T1和T2时,产物的量与反应时间的关系如右下图所示。则符合图示的正确判断是
2HI(g),在温度T1和T2时,产物的量与反应时间的关系如右下图所示。则符合图示的正确判断是