拆开1 mol化学键所吸收的能量是该化学键的键能,它的大小可以衡量化学键的强弱。
|
化学键 |
Si—O |
Si—Cl |
H—H |
H—Cl |
Si—Si |
Si—C |
|
键能/kJ·mol—1 |
460 |
360 |
436 |
431 |
176 |
347 |
下列说法中错误的是( )
A.SiCl4的熔点比SiC低
B.拆开1 mol晶体硅中的化学键所吸收的能量为176kJ
C.HCl的熔点比H2高
D.拆开1 mol晶体SiC中的化学键所吸收的能量为1388kJ
已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
|
电离能/kJ·mol—1 |
I1 |
I2 |
I3 |
I4 |
|
X |
578 |
1817 |
2745 |
11578 |
|
Y |
738 |
1451 |
7733 |
10540 |
|
Z |
496 |
4562 |
6912 |
9543 |
则X、Y、Z的电负性从大到小的顺序为( )
A.Z > Y > X B.X > Z > Y C.X > Y > Z D.Y > Z > X
下列对一些实验事实的理论解释正确的是 ( )。
|
选项 |
实验事实 |
理论解释 |
|
A |
氮原子的第一电离能大于氧原子 |
氮原子2p能级半充满 |
|
B |
CO2为直线形分子 |
CO2分子为非极性分子 |
|
C |
金刚石的熔点低于石墨 |
石墨熔融时除了破坏共价键,还需破坏范德华力 |
|
D |
HF的沸点高于HCl |
H-F的键能大于H-Cl |
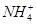 是等电子体,键角均为60°
是等电子体,键角均为60°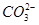 是等电子体,均为平面正三角形结构
是等电子体,均为平面正三角形结构