(7分)氮是地球上含量丰富的一种元素,氮元素的单质及其化合物在工农业生产、生活中有着重要作用。
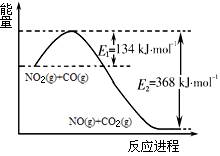
(1)根据右侧能量变化示意图,请写出NO2和CO反应的热化学方程式 。
(2)在固定体积的密闭容器中,进行如下化学反应:
N2(g)+3H2(g) 2NH3(g)
△H < 0 ,其平衡常数K与温度T的关系如下表:
2NH3(g)
△H < 0 ,其平衡常数K与温度T的关系如下表:
|
T/K |
298 |
398 |
498 |
|
平衡常数K |
4.1×106 |
K1 |
K2 |
①该反应的平衡常数表达式:K=
②试判断K1 K2(填写“>”,“=”或“<”)
③下列各项能说明该反应已达到平衡状态的是 (填字母)
a.容器内N2、H2、NH3的浓度之比为1∶3∶2
b.v(N2)正 = 3v(H2)逆
c.容器内压强保持不变
d.混合气体的密度保持不变
(3)对反应N2O4(g) 2NO2(g)
△H > 0 ,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示,下列说法正确的是
。
2NO2(g)
△H > 0 ,在温度分别为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如右图所示,下列说法正确的是
。
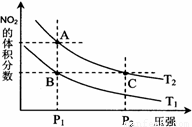
a.A、C两点的反应速率:A>C
b.A、C两点的化学平衡常数:A>C
c.A、C两点N2O4的转化率:A>C
d.由状态B到状态A,可以用加热的方法
㈠(2分)用pH试纸测定溶液pH的正确操作是 ______________________________________
㈡(7分)某校学生用中和滴定法测定某NaOH溶液的物质的量浓度,选甲基橙作指示剂。
⑴盛装0.2000 mol/L盐酸标准液应该用 式滴定管。
⑵滴定时,左手控制滴定管,右手摇动锥形瓶,眼睛注视_____________。
⑶ 滴定操作可分解为如下几步:
①检查滴定管是否漏水;
②取一定体积的待测液于锥形瓶中;
③用标准溶液润洗盛标准溶液的滴定管,用待测液润洗盛待测液的滴定管
④装标准溶液和待测液并调整液面(记录初读数)
⑤用蒸馏水洗涤玻璃仪器
⑥滴定操作
正确的操作顺序为: 。
⑷有关数据记录如下:则NaOH溶液的物质的量浓度为______________mol/L。
|
实验序号 |
待测液体积(mL) |
所消耗盐酸标准液的体积(mL) |
|
|
滴定前 |
滴定后 |
||
|
1 |
20.00 |
0.50 |
20.55 |
|
2 |
20.00 |
8.00 |
26.00 |
|
3 |
20.00 |
1.40 |
21.35 |
⑸滴定前平视读数,滴定终点时俯视读数,则会使所测碱的浓度值 。
(填“无影响”、“偏高”或“偏低”)。
(7分)过氧化氢对环境友好,性质多样,有很重要的研究和应用价值。
实验室利用反应2H2O2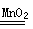 2H2O+O2↑可制备氧气。① 取等物质的量浓度等体积H2O2溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如下表所示。
2H2O+O2↑可制备氧气。① 取等物质的量浓度等体积H2O2溶液分别进行下列实验,研究外界条件对该反应速率的影响,实验报告如下表所示。
|
序号 |
条件 |
现象 |
结论 |
|
|
温度/℃ |
催化剂 |
|||
|
1 |
40 |
FeCl3溶液 |
|
|
|
2 |
20 |
FeCl3溶液 |
|
|
|
3 |
20 |
MnO2 |
|
|
|
4 |
20 |
无 |
|
|
实验1、2研究的是 对H2O2分解速率的影响。
实验2、3的目的是
实验中可以表明该反应速率差异的现象是
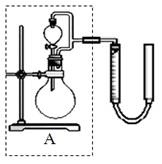
② 实验室用MnO2做该反应的催化剂,使用如右图所示装置的A部分制备O2,避免反应过于剧烈的操作是
 HCO3-+H+的平衡常数K1=
。(已知:10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=
。(已知:10-5.60=2.5×10-6) Al3++3OH-
B.NaHCO3 ===
Na++HCO3- HCO-3
Al3++3OH-
B.NaHCO3 ===
Na++HCO3- HCO-3
 ??2SO3(g),能增大正反应速率的措施是( )
??2SO3(g),能增大正反应速率的措施是( ) 2CO-Q1(吸热反应)反应速率为 u1,N2+3H2
2CO-Q1(吸热反应)反应速率为 u1,N2+3H2