(16分)金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝。高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:
WO3(s)+3 H2(g) W(s)+3 H2O(g)
W(s)+3 H2O(g)
请回答下列问题:
(1)上述反应的化学平衡常数表达式为
(2)某温度下反应达平衡时,随温度的升高, H2与水蒸气的体积比减小,则该反应为_____________反应(填 吸热或放热)
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
|
温度 |
25 ℃ ~ 550 ℃ ~ 600℃ ~ 700℃ |
|
主要成分 |
WO3 W2O5 WO2 W |
第一阶段反应的化学方程式为___________________________________________;580℃时,固体物质的主要成分为______ _________;,
(4)已知:温度过高时,WO2(s)转变为WO2(g);
WO2(s)+2 H2(g) W(s)+2H2O(g) ΔH=+66 kJ·mol-1
W(s)+2H2O(g) ΔH=+66 kJ·mol-1
WO2(g)+2 H2(g) W(s)+2H2O(g) ΔH= —137.9 kJ·mol-1
W(s)+2H2O(g) ΔH= —137.9 kJ·mol-1
则WO2(s) WO2(g)的ΔH=_____ _______.
WO2(g)的ΔH=_____ _______.
(5)钨丝灯管中的W在使用过程中缓慢挥发,使灯丝变细,加入I2可延长灯管的使用寿命,其工作原理为:

下列说法正确的有____________.
A.灯管内的I2可循环使用
B.WI4在灯丝上分解,产生的W又沉积在灯丝上
C.WI4在灯管壁上分解,使灯管的寿命延长
D.温度升高时, WI4的分解速率加快,W和I2的化合速率减慢
 H++OH-;ΔH>0,下列叙述正确的是
H++OH-;ΔH>0,下列叙述正确的是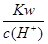 ="0.1"
mol/L的溶液:Na+、K+、SiO32-、NO3-
="0.1"
mol/L的溶液:Na+、K+、SiO32-、NO3- 2SO3(g),改变下列条件,可以提高反应物中活化分子百分数的是( )
2SO3(g),改变下列条件,可以提高反应物中活化分子百分数的是( ) 2C(g)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )
2C(g)。若经2 s(秒)后测得C的浓度为0.6 mol·L-1,现有下列几种说法,其中正确的是( )